

分析 (1)工业合成氨所需氮气来自空气,常用蒸馏空气的物理方法获得;原料气氢气中常含有少量CO、CO2、H2S等杂质,会引起催化剂中毒,必须除去;
(2)氮气和氢气在高温高压、催化剂条件下反应生成氨气,该反应在合成塔中进行,催化剂为铁触媒;
(3)NH3和CO2通入沉淀池中并加入CaSO4,生成(NH4)2SO4和CaCO3,发生CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4,得以发生的原因是沉淀转化的问题;
(4)根据氨在生产生活中的使用分析;
(5)碳酸钙高温下分解生成氧化钙和二氧化碳,二氧化碳可以循环利用,氧化钙为副产品;从反应原理及可循环利用物质、副产品及是否有污染物生成等角度分析;
(6)硫酸钙可以生产水泥石膏等.
解答 解:(1)工业合成氨所需氮气来自空气,常用蒸馏空气的物理方法获得;原料气氢气中常含有少量CO、CO2、H2S等杂质,会引起催化剂中毒,必须除去,
故答案为:蒸馏液态空气;防止催化剂中毒;
(2)氮气和氢气在高温高压、催化剂条件下反应生成氨气,该反应在合成塔中进行,
故答案为:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3;合成塔;
(3)NH3和CO2通入沉淀池中并加入CaSO4,生成(NH4)2SO4和CaCO3,发生CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4,得以发生的原因是碳酸钙的溶解性比硫酸钙小,有利于反应向正方向进行,
故答案为:CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4;生成碳酸钙溶解度小于硫酸钙,有利于反应向正向进行;
(4)上述生产流程中,氨气的作用是提供制各产品所需的氮元素,增大CO32-的浓度促进反应发生,不作为催化剂,
故答案为:AB;
(5))CaCO3在煅烧炉中分解生成CO2和CaO,CO2可循环使用,副产品为生石灰,根据反应流程离子,该反应的有利点为:生成的CO2可循环使用,CaO可制备硫酸钙,没有废物生成,
故答案为:CO2;该流程中产生的CO2循环使用,得到的产品和副产品都是有用的物质,无废物产生;
(6)硫酸钙的用途可以是生产水泥,石膏等,
故答案为:生产水泥,石膏.
点评 本题考查工业合成氨,题目难度中等,明确合成流程及反应原理为解答关键,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力,(2)为易错点,需要从难溶物溶解平均及其转化实质角度考虑.


 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:填空题
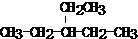 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电过程是电能转化为化学能的过程 | |
| B. | 充电时阳极反应:Ni(OH)2-e-+OH-═NiOOH+H2O | |
| C. | 放电时正极极附近溶液的pH变小 | |
| D. | 放电时电解质溶液中的OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
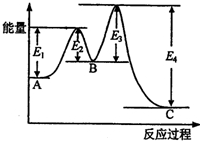 某反应由两步反应A?B?C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A?B?C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | 两步反应均为吸热反应 | B. | 稳定性C>A>B | ||
| C. | A与C的能量差为E4 | D. | A?C反应,反应条件一定要加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 侯氏制碱法是先将CO2通入饱和NaCl溶液后,再通入NH3 | |
| B. | 新型材料聚酯纤维、光导纤维都属于有机高分子材料 | |
| C. | PM2.5是指大气中直径≤2.5×10-6m的颗粒物(气溶胶),可通过加水吸收后再利用过滤的方法分离PM2.5微粒和可溶性吸附物 | |
| D. | “神十”航天服是由碳化硅陶瓷和碳纤维复合而制成的,它是一种新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.168L | B. | 0.112L | C. | 0.672L | D. | 0.224L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com