
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
(2)由表中数据可知,温度越高化学平衡常数越大,说明升高温度平衡向正反应移动,正反应是吸热反应;
(3)温度不变,平衡常数不变;
(4)反应前后气体不变,则增大压强平衡不移动;
(5)1200℃时,平衡常数为2.6,计算浓度幂,与2.6相比较可确定平衡移动方向.
解答 解:(1)可逆反应CO2(g)+H2(g)?CO(g)+H2O(g)的化学平衡常数表达式k=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$,故答案为:$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)由表中数据可知,温度越高化学平衡常数越大,升高温度平衡向正反应移动,正反应是吸热反应,故答案为:吸热;
(3)温度不变,平衡常数不变,则平衡常数等于1,故答案为:等于;
(4)反应前后气体不变,则增大压强平衡不移动,故答案为:不;
(5)若1200℃时,在某时刻该容器中CO2、H2、CO、H2O的浓度分别为2mol•L-1、2mol•L-1、4mol•L-1、4mol•L-1,则$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$=$\frac{4×4}{2×2}$=4>2.6,则平衡逆向移动,故答案为:逆反应方向.
点评 本题考查化学平衡计算,为高频考点,侧重于学生的分析能力和计算能力的考题,题目涉及平衡常数计算、影响因素及应用等,难度中等,注意掌握化学平衡常数的应用和意义.


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源:2017届广东省山一高三上第二次统测化学试卷(解析版) 题型:选择题
某含Na+的溶液中可能含有NH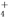 、Fe3+、Br-、CO
、Fe3+、Br-、CO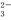 、I-、SO
、I-、SO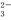 。取样,滴加足量氯水,有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液或淀粉均无现象。为确定该溶液的组成,还需进行的实验有( )
。取样,滴加足量氯水,有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液或淀粉均无现象。为确定该溶液的组成,还需进行的实验有( )
A.取样,滴加硫氰化钾溶液
B.取样,加氯水和CCl4,振荡
C.取样,加足量盐酸加热,湿润的品红试纸检验气体
D.取样,加足量的熟石灰加热,湿润的红色石蕊试纸检验气体
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
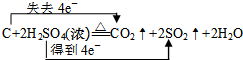 .
.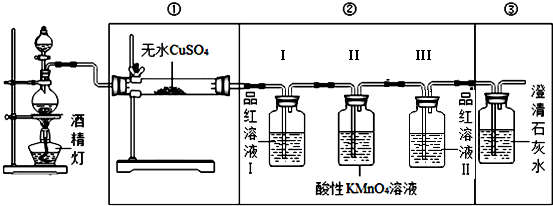
| 实验装置 | ① | ③ |
| 实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 温度/°C | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

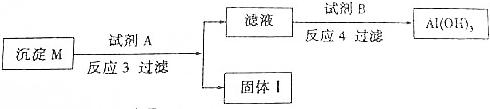
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
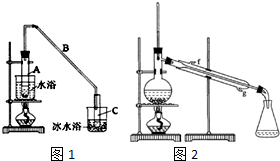 某化学小组采用类似乙酸乙酯的装置如图1:以环己醇制备环己烯.
某化学小组采用类似乙酸乙酯的装置如图1:以环己醇制备环己烯.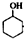 $→_{85℃}^{稀H_{2}SO_{4}}$
$→_{85℃}^{稀H_{2}SO_{4}}$ +H2O
+H2O| 密度(g.cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.096 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.081 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
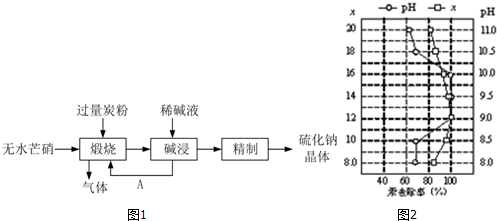
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
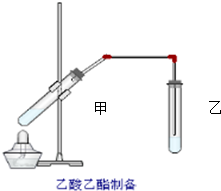 如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com