
| A、白铁(镀锌铁) |
| B、马口铁(镀锡铁) |
| C、镀金铁 |
| D、镀铜铁 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| A、172.5 kJ |
| B、1 149 kJ |
| C、283 kJ |
| D、566 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4HCO3和盐酸的反应是放热反应 |
| B、该反应中,热能转化为产物内部的能量 |
| C、反应物的总能量高于生成物的总能量 |
| D、反应的热化学方程式为NH4HCO3+HCl-→NH4Cl+CO2↑+H2O△H=+Q kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 硫、氯及其化合物由广泛的用途.
硫、氯及其化合物由广泛的用途.| 资料:25℃ H2CO3 Kal=4.4×10-7 H2S Kal=1.3×10-7 H2SO3 Kal=1.54×10-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在常温常压下,11.2 L N2含有的分子数为0.5 NA |
| B、在常温常压下,1 mol Ne含有的原子数为NA |
| C、1 L 1 mol/L醋酸溶液中离子总数为2NA |
| D、18 g水中所含的电子数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②③④⑤ |
| C、③④ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
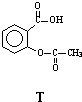
| A、T可以发生酯化反应 |
| B、T可以与NaOH溶液反应 |
| C、T属于芳香烃类化合物 |
| D、T在酸中水解可以得到CH3COOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com