
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全。确定分解产物的成分。

(1)B装置的作用是_________。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中一定有_______气体产生,写出D中发生反应的离子方程式________。
(3)A中固体分解后产生NH3,写出其两种用途_________。
(4)用实验的方法验证C溶液含有NH4+:_________。
【答案】检验产物中是否有水生成 SO2 SO2+H2O2+Ba2+=BaSO4↓+2H+ 制冷剂,作氮肥 取少量C溶液于洁净的试管中,加入浓NaOH并加热,若产生的气体能使湿润的红色石蕊试纸变蓝,说明C溶液含有NH4+,反之,则无NH4+存在。
【解析】
水蒸气能使无水硫酸铜变蓝色,用无水硫酸铜检验水蒸气;盐酸酸化的氯化钡溶液能和三氧化硫反应生成硫酸钡沉淀,双氧水能氧化二氧化硫生成硫酸,硫酸和氯化钡溶液反应生成硫酸钡沉淀,所以C检验三氧化硫、D检验二氧化硫,且生成的氨气能和HCl反应生成铵盐,用水处理尾气;
(1)无水硫酸铜检验水蒸气;
(2)三氧化硫和氯化钡生成硫酸钡沉淀,二氧化硫和氯化钡溶液不反应;双氧水具有氧化性,能氧化二氧化硫生成硫酸,硫酸能和氯化钡在溶液中反应生成硫酸钡沉淀;
(3)氨气能作制冷剂、做氮肥;
(4)能使湿润的红色石蕊试纸变蓝色的气体是氨气,先用铵根离子转化为氨气,然后再用湿润的红色石蕊试纸检验氨气,则可以用于铵根离子的检验。
(1)水蒸气能使无水硫酸铜溶液变蓝色,用无水硫酸铜检验水蒸气,则B装置的作用是检验产物中是否有水生成,如果有水,则无水硫酸铜变蓝色;
(2)实验中,观察到C中盐酸酸化的氯化钡溶液中无明显现象,证明无SO3生成,D中H2O2具有氧化性,在酸性条件下能氧化SO2生成H2SO4,H2SO4电离产生的SO42-与溶液中的Ba2+结合生成BaSO4白色沉淀,有白色沉淀生成,可确定产物中一定有SO2,D中反应的离子方程式为:SO2+H2O2+Ba2+=BaSO4↓+2H+;
(3)A中硫酸亚铁铵[(NH4)2Fe(SO4)2]受热分解产生NH3,液氨气化需要吸收热量导致其周围环境温度降低,所以能作制冷剂,N元素是农作物生长需要的营养元素,还可以作氮肥;
(4)用实验的方法验证C溶液含有NH4+:取少量C溶液于洁净的试管中,加入浓NaOH并加热,若产生的气体能使湿润的红色石蕊试纸变蓝,说明C溶液含有NH4+,反之,则无NH4+存在。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】8.34 g FeSO4·7H2O(相对分子质量:278)样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示,下列说法正确的是
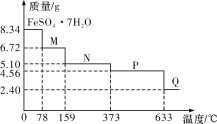
A.温度为78 ℃时固体物质M的化学式为FeSO4·5H2O
B.温度为159 ℃时固体N的化学式为FeSO4·2H2O
C.取适量380 ℃时所得的样品P,隔绝空气加热至650 ℃,得到一种固体物质Q,同时只得到一种无色气体生成
D.在隔绝空气条件下,N得到P的化学方程式为FeSO4·H2O![]() FeSO4+H2O
FeSO4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl为白色粉末,微溶于水,不溶于乙醇,潮湿的CuCl在空气中被氧化为Cu2(OH)3Cl。
(1)一种由海绵铜(Cu)为原料制备CuCl的工艺流程如下:
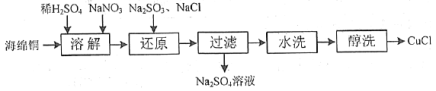
①“溶解”步骤发生反应的离子方程式为_________________________________;
②潮湿的CuCl在空气中被氧化的化学反应方程式为_________________________________;
③已知常温下Cu(OH)2溶度积常数Ksp=2×10-20要使c(Cu2+)=0.2 mol·L-1的硫酸铜溶液中的铜离子沉淀比较完全(使铜离子浓度变为原来的千分之一)则应调节溶液pH为___________以上。
(2)次磷酸(H3PO2)是一元中强酸,可用于作金属表面处理剂。
①向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,写出反应的化学方程式:_____________;
②H3PO2可将溶液中的Ag+还原为银,从而用于化学镀银,反应同时生成P元素最高价氧化物对应的水化物。在该过程中,氧化剂与还原剂的物质的量之比为:___________;
③NaH2PO2的水溶液呈弱碱性,用离子方程式说明原因:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用有机物甲可制备环己二烯(![]() ),其反应路线如图所示:
),其反应路线如图所示:

下列有关判断不正确的是
A.甲的分子式为 C6H12
B.乙与环己二烯互为同系物
C.上述流程发生的反应类型有取代反应、消去反应、加成反应
D.环己二烯与溴水 1:1 反应可得 2 种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W是否位于同一周期(填“是”或“否”):__________,理由是________________。
(2)Y是_______,Z是_______,W是_______。
(3)X、Y、Z和W可组成一种化合物,其原子个数比为8∶2∶4∶1,写出该化合物的名称及化学式: _______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据部分短周期元素的信息回答问题。
元素 | 元素信息 |
A | 第3周期ⅣA族 |
B | 族序数是周期数的3倍 |
C | 原子序数是11 |
D | D3+与Ne的电子数相同 |
(1)A、B的元素符号分别为__、__,C、D的元素名称分别为__、__。
(2)写出B、C的常见单质在加热时的反应方程式:__。
(3)从原子结构的角度分析,A原子与B原子的__相同,C原子与D原子的__相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白黎芦醇具有抗氧化和预防心血管疾病的作用,下列有关白黎芦醇的说法正确的是( )

A.白黎芦醇能与NaHCO3溶液反应
B.分子中共含有7种化学环境不同的氢原子
C.1mol白黎芦醇最多能与7mol氢气加成
D.1mol白黎芦醇最多能反应溴水中的3.5mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会第26届会议修订了阿伏加德罗常数(NA=6.02214076×1023mol-1),于2019年5月2日正式生效。设NA是阿伏加德罗常数的值,下列说法正确的是
A.40g正丁烷和18 g异丁烷的混合物中共价键数目为13NA
B.常温常压下,124 g P4中所含P—P键数目为4NA
C.电解精炼铜时,阳极质量减小3.2g时,转移的电子数为0.1NA
D.0.1mol FeCl3完全水解转化为氢氧化铁胶体,生成胶粒数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的许多植物中含有醛,其中有些具有特殊香味,可作为植物香料使用,例如桂皮含肉桂醛(![]() ),杏仁含苯甲醛(
),杏仁含苯甲醛(![]() )。下列说法错误的是( )
)。下列说法错误的是( )
A.肉桂醛和苯甲醛都能发生加成反应、取代反应
B.可用新制氢氧化铜悬浊液检验肉桂醛分子中的含氧官能团
C.肉桂醛和苯甲醛互为同系物
D.苯甲醛分子中所有原子可能位于同一平面内
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com