
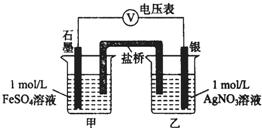
 为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验:
为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验:| 序号 | 操作 | 现象 |
| 实验Ⅰ | 将2mL1mol/L AgNO3溶液加入到 1mL1mol/L FeSO4溶液中 | 产生白色沉淀,随后有黑色固体产生 |
| 取上层清液,滴加KSCN溶液 | 溶液变红 |
| 序号 | 操作 | 现象 |
| 实验Ⅲ | 将2mL2mol/LFe(NO3)3溶液加入有银镜的试管中 | 银镜消失 |
| 实验Ⅳ | 将2mL1mol/LFe2(SO4)3溶液加入有银镜的试管中 | 银镜减少,未消失 |
| 实验Ⅴ | 将2mL2mol/LFeCl3溶液加入有银镜的试管中 | 银镜消失 |
分析 (1)将2mL 1mol/L AgNO3溶液加入到1mL 1mol/L FeSO4溶液中分数复分解反应会生成硫酸银白色沉淀,银离子具有强氧化性会氧化Fe2+为Fe3+,银离子被还原为黑色固体金属单质银;取上层清液,滴加KSCN溶液溶液变红说明有铁离子生成;
(2)①偏移的方向表明:电子由石墨经导线流向银,银做原电池正极,石墨做原电池负极,甲池溶液中是亚铁离子失电子发生氧化反应生成铁离子,;
②随后向甲烧杯中逐渐加入浓Fe2(SO4)3溶液,和乙池组成原电池,发现电压表指针的变化依次为,偏移减小→回到零点→逆向偏移,证明银做原电池负极,发生的反应为铁离子氧化为银;
③实验可知银离子具有强氧化性氧化亚铁离子为铁离子;
(3)①酸性溶液中硝酸根离子具有氧化性,也可以溶解银;
②分析选项可知,溶液中存在平衡:Fe3++Ag=Fe2++Ag+,硫酸根离子和氯离子对平衡的影响判断平衡进行的方向解释,AgCl比Ag2SO4溶解度更小,Cl-比SO42-更有利于降低Ag+浓度,所以实验Ⅴ比实验Ⅳ正向进行的程度更大.
解答 解:(1)将2mL 1mol/L AgNO3溶液加入到1mL 1mol/L FeSO4溶液中分数复分解反应会生成硫酸银白色沉淀,银离子具有强氧化性会氧化Fe2+为Fe3+,银离子被还原为黑色固体金属单质银;取上层清液,滴加KSCN溶液溶液变红说明有铁离子生成;
①上述分析可知白色沉淀为硫酸银,它的化学式是Ag2SO4,
故答案为:Ag2SO4;
②甲同学得出Ag+氧化了Fe2+的依据是实验现象中,银离子被还原为黑色固体金属单质银,取上层清液,滴加KSCN溶液溶液变红说明有铁离子生成,
故答案为:有黑色固体(Ag)生成,加入KSCN溶液后变红;
(2)①实验过程中电压表指针偏移,偏移的方向表明:电子由石墨经导线流向银,依据原电池原理可知银做原电池正极,石墨做原电池负极,负极是甲池溶液中亚铁离子失电子发生氧化反应生成铁离子,a中甲烧杯里的电极反应式是Fe2+-e-=Fe3+;
故答案为:Fe2+-e-=Fe3+;
②随后向甲烧杯中逐渐加入浓Fe2(SO4)3溶液,和乙池组成原电池,发现电压表指针的变化依次为,偏移减小→回到零点→逆向偏移,依据电子流向可知乙池中银做原电池负极,发生的反应为铁离子氧化为银生成亚铁离子;
故答案为:负;
③由实验现象得出,Ag+和Fe2+反应生成铁离子和金属银,反应的离子方程式是Fe2++Ag+?Fe3++Ag;
故答案为:Fe2++Ag+?Fe3++Ag;
(3)①将2mL 2mol/L Fe(NO3)3溶液加入有银镜的试管中银镜消失,说明银杯氧化,可能是溶液中铁离子的氧化性,也可能是铁离子水解显酸性的溶液中,硝酸根离子在酸溶液中具有了强氧化性,稀硝酸溶解银,所以实验Ⅲ不能证明Fe3+氧化了Ag,
故答案为:不能;因为Fe(NO3)3溶液呈酸性,酸性条件下NO3-也可能氧化Ag;
②将2mL1mol/L Fe2(SO4)3溶液加入有银镜的试管中银镜减少,未消失说明部分溶解,将2mL 2mol/L FeCl3溶液加入有银镜的试管中银镜消失,说明银溶解完全,依据上述现象可知,溶液中存在平衡:Fe3++Ag?Fe2++Ag+,且AgCl比Ag2SO4溶解度更小,Cl-比SO42-更有利于降低Ag+浓度,(或AgCl比Ag2SO4 Ksp(或溶解度)更小,促使平衡正向移动,银镜溶解).所以实验Ⅴ比实验Ⅳ正向进行的程度更大,
故答案为:溶液中存在平衡:Fe3++Ag?Fe2++Ag+,且 AgCl比Ag2SO4 Ksp(或溶解度)更小,Cl-比SO42-更有利于降低Ag+浓度,所以实验Ⅴ比实验Ⅳ正向进行的程度更大.(或AgCl比Ag2SO4 Ksp(或溶解度)更小,促使平衡正向移动,银镜溶解).
点评 本题考查了物质性质的实验设计验证,物质性质的理解,原电池原理分析,主要是实验现象和反应产物分析判断,注意题干信息的理解应用,掌握化学平衡知识是关键,题目难度较大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | A、B、E一定处于1、2、3三个不同周期 | |
| B. | A、D不可能在同一主族 | |
| C. | C的最高氧化物的水化物可能显碱性 | |
| D. | C和D的单质不可能化合成1:1型离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al$\stackrel{氧气,加热}{→}$Al2O3$\stackrel{硝酸}{→}$Al(NO3)3$\stackrel{加热蒸干}{→}$硝酸铝晶体 | |
| B. | Cu$\stackrel{氧气,加热}{→}$CuO$\stackrel{稀硫酸}{→}$CuSO4$\stackrel{蒸干结晶}{→}$胆矾 | |
| C. | Fe$\stackrel{氯气}{→}$FeCl3$\stackrel{过量氨水}{→}$Fe(OH)3$\stackrel{加热}{→}$Fe2O3 | |
| D. | FeSO4溶液$\stackrel{硫化氢、过滤}{→}$FeS |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
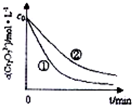 某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr2+.某课题组研究发现,少量铁明矾[Al2Fe(SO4)4•4H2O]即可对该反应起催化作用,为进一步研究有关因素对该反应速率的影响,探究如下:
某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr2+.某课题组研究发现,少量铁明矾[Al2Fe(SO4)4•4H2O]即可对该反应起催化作用,为进一步研究有关因素对该反应速率的影响,探究如下:| 实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
| ① | 4 | a=60 | 10 | 30 |
| ② | 5 | 60 | 10 | c=30 |
| ③ | 5 | 60 | b=20 | 20 |
| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
| 取等物质的量的K2SO4•Al2(SO4)3•24H2O代替实验①中的铁明矾,控制其他反条件与实验①相同,进行对比实验. | 反应进行相同时间后, 若溶液中的Cr2O72-浓度大于 实验①中的Cr2O72的浓度,则假设一成立; 若溶液中的Cr2O72-浓度等于 实验①中的Cr2O72的浓度,则假设一不成立. |
| 组数 | 1 | 2 | 3 | 4 |
| 消耗V(KMnO4)/ml | 20.04 | 20.00 | 18.90 | 19.96 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (c-a-b)kJ | B. | (a+b-c)kJ | C. | (2c-a-b)kJ | D. | $\frac{2c-a-b}{2}$kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 强电解质 | HF | HClO4 | Ba(OH)2 | 食盐水溶液 |
| 弱电解质 | Cu(OH)2 | NH3•H2O | BaSO4 | HClO |
| 非电解质 | Cu | SO2 | 蔗糖 | H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com