
下列说法正确的是
A.离子键是指阴阳离子间的静电引力
B.离子化合物是指只含有离子键的化合物
C.升高温度只能使吸热反应的速率增大,不能使放热反应的速率增大
D.粉碎固体反应物可以增大反应速率
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年河南省周口市高二下学期期中考试化学试卷(解析版) 题型:填空题
蚂蚁等昆虫蛰人时,向人体内注入一种有机物A造成疼痛.为探究该物质的结构与性质,某研究性学习小组设计了下列实验:
实验一:收集蚂蚁经处理后进行蒸馏,获得一定量的无色液体A.
实验二:质谱分析显示,A物质的最大质荷比为46;核磁共振氢谱表明,A物质核磁共振氢谱有两种氢原子吸收峰,且峰面积之比为1:1;红外光谱图发现存在C=O键、C﹣O键等化学键的振动吸收.
请参与探究并回答相关问题:
(1)蒸馏时,除冷凝管、牛角管、锥形瓶、酒精灯、温度计外,还用到的玻璃仪器是 ,
(2)写出A物质的结构简式: ,官能团的名称 ___
(3)在确定A的结构后,该研究性学习小组猜想A可能具有酸性.请你设计出至少一个实验方案来验证A的酸性: .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高二下第十二周练化学卷(解析版) 题型:选择题
已知含氧酸可用通式XOn(OH)m来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中n大的是强酸,n小的是弱酸。下列各含氧酸中酸性最强的是
A.H2SeO3 B.HMnO4 C.H3BO3 D.H3PO4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次增大的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2型分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g/L,W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A.原子半径:W>Z>Y>X>M
B.XZ2、M2Z2、W2Z2均为共价化合物
C.由X元素形成的单质不一定能导电
D.由Y、Z、M三种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
下列各组的电极材料和电解液,不能组成原电池的是
A.铜片、铜片、稀硫酸 B.铜片、石墨棒、硝酸银溶液
C.锌片、铜片、稀硫酸 D.铜片、银片、FeCl3溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中理科化学试卷(解析版) 题型:填空题
四苯基乙烯(TPE)及其衍生物具有聚集诱导发光特性,在光电材料等领域应用前景广阔。以下是TPE的合成路线(部分试剂和反应条件省略):

(1)A的名称是 ;试剂Y为 。
(2)B→C的反应类型是 ;B中官能团的名称是 ; D中官能团的名称 。
(3)E→F的化学方程式是 。
(4)W是D的同分异构体,具有下列结构特征:属于萘( )的一元取代物;存在羟甲基(—
)的一元取代物;存在羟甲基(—
CH2OH)。写出W所有可能的结构简式: 。
(5)下列说法正确的是 ( )
a.B的酸性比碳酸强 b.D不能发生还原反应
c.E含有3种不同化学环境的氢 d.TPE既属于芳香烃也属于烯烃
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中理科化学试卷(解析版) 题型:选择题
合成导电高分子材料PPV的反应:
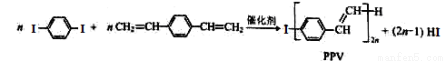
下列说法中正确的是
A.合成PPV的反应为加聚反应
B.PPV与聚苯乙烯具有相同的重复结构单元
C.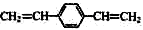 和苯乙烯互为同系物
和苯乙烯互为同系物
D.通过质谱法测定PPV的平均相对分子质量,可得其聚合度
查看答案和解析>>
科目:高中化学 来源:2016届西藏日喀则一中高三下学期二模考试理综化学试卷(解析版) 题型:填空题
氮及其化合物与人类生产、生活息息相关.回答下列问题:
(1)基态N原子中电子在2p轨道上的排布遵循的原则是__________,前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为__________。
(2)C、N、O三种元素第一电离能从大到小的顺序是__________。
(3)N2F2分子中N原子的杂化方式是__________,l mol N2F2含有__________molσ键.
(4)NF3的键角__________NH3的键角(填“<”“>”或“=”),原因是__________.
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.l mol NH4BF4__________mol配位键.
(6)安全气囊的设计原理为6NaN3+FeIO3 Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑
①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质.写出两种与N3-互为等电子体的分子或离子__________.
②Na2O的晶胞结构如图所示,品胞边长为566pm,晶胞中氧原子的配位数为__________,Na2O晶体的密度为__________g•cm-3(只要求列算式,不必计算出结果)。

查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三第四次模拟理综化学试卷(解析版) 题型:选择题
C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该电池的电池反应式为:NaMO2+nC?Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )
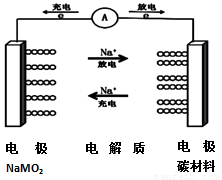
A.电池放电时,溶液中钠离子向负极移动
B.该电池负极的电极反应为:NaMO2-xe-═Na(1-x)MO2+xNa+
C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D.电池充电时的阳极反应式为:nC+x Na+-xe-═NaxCn
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com