
【题目】回答下列各题:
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol,
②![]()
![]() ,
,
③![]()
![]()
则表示氢气燃烧热的热化学方程式为________。
(2)判断下列反应的熵值是增大、减小还是几乎不变。
①2H2(g)+O2(g)=2H2O(l);熵 ________(填“增大”“减小”“几乎不变”,下同)
②H2(g)+Cl2(g)=2HCl(g);熵________
③(NH4)2CO3(g)=NH4HCO3(g)+NH3(g);熵________
④Cu(s)+Cl2(g)=CuCl2(s);熵________
【答案】H2(g)+![]() O2(g)=H2O(l)△H=-124.6kJ/mol 减小 几乎不变 增加 减小
O2(g)=H2O(l)△H=-124.6kJ/mol 减小 几乎不变 增加 减小
【解析】
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol,②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol,③H2O(l)=H2O(g)△H=+44kJ/mol,根据盖斯定律,(②-①)÷3-③可得:H2(g)+
O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol,③H2O(l)=H2O(g)△H=+44kJ/mol,根据盖斯定律,(②-①)÷3-③可得:H2(g)+![]() O2(g)=H2O(l);
O2(g)=H2O(l);
(2)产生气体或气体物质的物质的量增大的反应,熵变通常都是正值,为熵增加反应,反之为熵减小的反应,据此判断。
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol,②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol,③H2O(l)=H2O(g)△H=+44kJ/mol,根据盖斯定律,(②-①)÷3-③可得:H2(g)+
O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol,③H2O(l)=H2O(g)△H=+44kJ/mol,根据盖斯定律,(②-①)÷3-③可得:H2(g)+![]() O2(g)=H2O(l)则△H=[( -192.9kJ/mol)-( +49.0kJ/mol)]÷3-(+44kJ/mol) = -124.6kJ/mol,即氢气燃烧热的热化学方程式为H2(g)+
O2(g)=H2O(l)则△H=[( -192.9kJ/mol)-( +49.0kJ/mol)]÷3-(+44kJ/mol) = -124.6kJ/mol,即氢气燃烧热的热化学方程式为H2(g)+![]() O2(g)=H2O(l)△H=-124.6kJ/mol;
O2(g)=H2O(l)△H=-124.6kJ/mol;
(2)①2H2(g)+O2(g)═2H2O(l)为气体体积减小的反应,属于熵值减小的反应;
②H2(g)+Cl2(g)═2HCl(g)前后气体体积不变,熵值几乎不变;
③(NH4)2 CO3(s)═NH4HCO3(s)+NH3(g),反应前没有气体,反应后生成气体,为熵值增加的反应;
④Cu(s)+Cl2(g)═CuCl2(s),反应前有气体,反应后没有气体,属于熵值减小的反应。


科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g)![]() CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
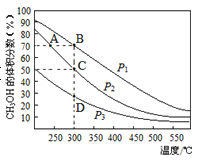
A. 该反应的△H<0,且p1<p2
B. 反应速率:ν逆(状态A)>ν逆(状态B)
C. 在C点时,CO转化率为75%
D. 在恒温恒压条件下向密闭容器中充入不同量的CH3OH,达平衡时CH3OH的体积分数也不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,可逆反应C(s)+CO2(g)![]() 2CO(g),达到平衡状态的标志是( )
2CO(g),达到平衡状态的标志是( )
①单位时间内生成n molCO2的同时生成n molC ②单位时间内生成n molCO2 的同时生成2n mol CO ③CO2 、CO的物质的量浓度之比为1: 2的状态 ④混合气体的密度不再改变的状态 ⑤混合气体的压强不再改变的状态 ⑥C的质量不再改变的状态
A. ①④⑤⑥ B. ②④⑤⑥ C. ②③⑤⑥ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按下列要求填空:
(1)已知,NaBH4与水反应:BH4- +2H2O=BO2-+4H2↑(反应实质为水电离出来的H+被还原),反应后所得溶液显碱性,用离子方程式表示出溶液显碱性的原因___________________________________。
(2)广义的水解观认为:水解的物质和水分别离解成两部分,然后两两重新结合成新的物质,不出现元素化合价的变化.根据以上信息,下列物质水解后的产物错误的是 ___________
①BaO2的水解产物是Ba(OH)2和H2O2 ②PCl3水解的产物是HClO和PH3
③CaC2水解的产物是Ca(OH)2和C2H2 ④Al2S3水解的产物是Al(OH)3和H2S
⑤TiCl4水解产物是TiO2·xH2O和HCl
(3)化学反应可为人类提供能量。已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1 = -a kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2 = -b kJ/mol
③ H2O(g)= H2O(l) ΔH3 = -c kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_____________________
(4)常温下,浓度均为0.1mol·L-1的下列五种钠盐溶液的pH如下表;
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
上述盐溶液中的阴离子,结合H+能力最强的是_________,根据表中数据,浓度均为0.01mol·L—1的下列四种酸的溶液分别稀释100倍,pH变化最大的是_______。
A.HCN B.HClO C.CH3COOH D.H2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.比例模型![]() :可以表示二氧化碳分子,也可以表示水分子
:可以表示二氧化碳分子,也可以表示水分子
B.室温下,将![]() HA溶液和
HA溶液和![]() 溶液等体积混合
溶液等体积混合![]() 忽略混合时溶液体积的变化
忽略混合时溶液体积的变化![]() 测得混合溶液的
测得混合溶液的![]() ,则混合溶液中由水电离出的
,则混合溶液中由水电离出的![]()
C.纯碳新材料“碳纳米泡沫”,每个泡沫含有约4000个碳原子,直径约6到9nm,在低于![]() 时,泡沫具有永久磁性,“碳纳米泡沫”与石墨互为同位素
时,泡沫具有永久磁性,“碳纳米泡沫”与石墨互为同位素
D.已知![]() 的
的![]() 为
为![]() ,则将等体积的
,则将等体积的![]()
![]() 的
的![]() 溶液和
溶液和![]()
![]() 溶液混合,不会有
溶液混合,不会有![]() 沉淀产生
沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是![]()
A.地下钢铁管道用导线连接铜块可以减缓管道的腐蚀
B.反应![]() 的熵变
的熵变![]()
C.常温下,![]() ,
,![]() 的含
的含![]() 溶液中,
溶液中,![]()
D.![]() 时,
时,![]() 的
的![]() 溶液与等浓度的
溶液与等浓度的![]() 溶液的导电能力相同
溶液的导电能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,加入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+mY(g)![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为60%、30%、10%。在此平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
3Z(g),平衡时,X、Y、Z的体积分数分别为60%、30%、10%。在此平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
A.m=1B.第二次平衡时,Y的浓度为1.2 mol·L-1
C.两次平衡的平衡常数相同D.X与Y的平衡转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告指出:“坚持全民共治、源头防治,持续实施大气污染防治,打赢蓝天保卫战!”以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
(1)工业上采用NH3-SCR法是消除氮氧化物的常用方法。它利用氨在一定条件下将NOx在脱硝装置中转化为N2。主要反应原理为:
主反应:a. 4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) ΔH1;
4N2(g)+6H2O(g) ΔH1;
副反应:b. 4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) ΔH2=-1267.1kJ/mol;
2N2(g)+6H2O(g) ΔH2=-1267.1kJ/mol;
c. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH3=-907.3kJ/mol
4NO(g)+6H2O(g) ΔH3=-907.3kJ/mol
①主反应的ΔH1=____________。
②将氮氧化合物按一定的流速通过脱硝装置,测得出口的NO残留浓度与温度的关系如图所示,试分析脱硝的适宜温度是______(填序号)。

a.<850℃ b.900~1000℃ c.>1050℃
温度超过1000℃,NO浓度升高的原因是_______________。
(2)已知:8NH3(g)+6NO2(g)![]() 7N2(g) +12H2O(l) ΔH<0。相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间变化如上如图所示。该反应活化能Ea(A)、Ea(B)、Ea(C)由小到大的顺序是____________,理由是___________。
7N2(g) +12H2O(l) ΔH<0。相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间变化如上如图所示。该反应活化能Ea(A)、Ea(B)、Ea(C)由小到大的顺序是____________,理由是___________。

(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH=-746.8kJ·mol-1,实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。若在1L的密闭容器中充入1mol CO和1mol NO,在一定温度下达到平衡时,CO的转化率为40%,则
N2(g)+2CO2(g) ΔH=-746.8kJ·mol-1,实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。若在1L的密闭容器中充入1mol CO和1mol NO,在一定温度下达到平衡时,CO的转化率为40%,则![]() =___________。(用分数表示)
=___________。(用分数表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO- + Cl- + 2H+ = Cl2↑+ H2O。某学习小组拟探究该消毒液的变质情况。
(1)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过下列装置检验气体的成分可以判断消毒液是否变质。
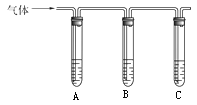
学习小组研究后认为变质情况可能有三种:甲:部分变质;乙:未变质;丙:______。
为了验证可能为甲,请完成下列实验方案。限选试剂:
a.98%的浓硫酸 b.1%的品红溶液 c.1.0 mol·L-1的KI-淀粉溶液
d.1.0 mol·L-1 的NaOH溶液 e.澄清石灰水 f.饱和NaCl溶液
所加试剂 | 预期现象和结论 |
试管A中加足量______(填序号); 试管B中加1%品红溶液; 试管C中加______(填序号)。 | 若A中________, B中________, C中________,则甲成立。 |
(2)用滴定法测定消毒液中NaClO的浓度。
①在使用滴定管之前首先进行的操作是_____________________;
②量取25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液v1 mL;(反应的化学方程式为:NaClO + Na2SO3 = NaCl+ Na2SO4)将b mol·L-1的用硫酸酸化的KMnO4溶液装入_________(填仪器名称)中;滴定剩余的Na2SO3溶液,反应的化学方程式为:_______________。当溶液由__________(填滴定终点现象)停止滴定,记录数据。
③重复上述滴定操作2次,平均消耗酸性KMnO4溶液v2 mL。则消毒液中NaClO的浓度为_______mol·L-1(用含a、b、v1、v2的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com