
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.6g固体;向上述滤液中加足量BaCl2溶液,得到 4.66g不溶于盐酸的沉淀。由此可知原溶液中
A.至少存在5种离子
B.Cl-一定存在,且c(Cl-)≥0.4mol/L
C.SO42-、NH4+、一定存在,Cl-可能不存在
D.CO32-、Al3+一定不存在,K+可能存在
B
【解析】
试题分析:由于加入过量NaOH溶液,加热,得到0.02mol气体,说明一定有NH4+,且物质的量为0.02mol;同时产生红褐色沉淀,说明一定有Fe3+,1.6g固体为氧化铁,物质的量为0.01mol,故有0.02molFe3+,一定没有CO32-;4.66g不溶于盐酸的沉淀为硫酸钡,一定有SO42-,物质的量为0.02mol;根据电荷守恒,一定有Cl-,至少 0.02mol×3+0.02-0.02mol×2=0.04mol,物质的量浓度至少0.04mol÷0.1L=0.4mol/L,A、至少存在Cl-、SO42-、NH4+、Fe3+四种离子,故A错误;B、根据电荷守恒,至少存在0.04molCl-,故B正确;C、一定存在氯离子,故C错误;D、Al3+无法判断是否存在,故D错误;故选B。
考点:考查离子共存知识


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015届河南省高二上学期期中考试化学试卷(解析版) 题型:选择题
已知:C(s)+O2(g)=CO2 (g) △H1
CO2(g)+C(s)=2CO(g) △H2
2CO(g)+O2(g)=2CO2(g) △H3
4Fe(s)+3O2(g)=2Fe2O3(s) △H4
3 CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s) △H5
下列关于上述反应焓变的判断正确的是
A.△H1>0,△H3<0 B.△H2>0,△H3>0
C.△H1=△H2+△H3 D.△H3=△H4+△H5
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高三上学期摸底考试化学试卷(带析版) 题型:实验题
(8分)硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
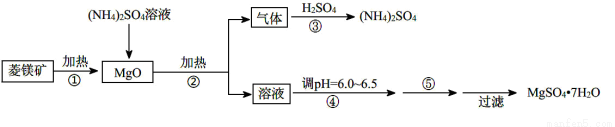
(1)步骤②中发生反应的离子方程式为 。
(2)步骤④中调节pH=6.0~6.5的目的是 。
(3)步骤⑤的操作为
(4)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为 [25℃时,Ksp[Mg(OH)2] =5.6×10-12]。
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高三上学期摸底考试化学试卷(带析版) 题型:选择题
下表各组物质之间通过一步反应不可以实现如下图所示转化关系的是
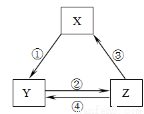
选项 | X | Y | Z | 箭头上所标 数字的反应条件 |
A | Na2O2 | NaOH | NaCl | ① 常温遇水 |
B | AlCl3 | NaAlO2 | Al(OH)3 | ② 通入CO2 |
C | NO | NO2 | HNO3 | ④ 加入铜粉 |
D | Cl2 | NaClO | HClO | ③ 加浓盐酸 |
查看答案和解析>>
科目:高中化学 来源:2015届河北省衡水市高三上学期第一次月考化学试卷(解析版) 题型:填空题
(本题共10分)(一)(6分)中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出)。单质A常作为食品包装材料,甲是两性氧化物。

根据图示转化关系回答:
(1)写出下列物质的化学式:单质A_______________,乙_______________。
(2)写出单质A与Fe2O3反应的化学方程式: ,利用该反应的原理,可用于______________________________。
(3)用单质A做成的容器可以储存和运输浓硫酸的原因是____________________________。
(4)写出反应①的离子方程式:_____________________________________________。
(二)(4分)(5)工业上冶炼下列物质通常不采用电解法的是 。
a.Na b.Mg c.Fe d.Ag
(6)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有( )
a.KCl b. KClO 3 c. MnO2 d. Mg
查看答案和解析>>
科目:高中化学 来源:2015届河北省衡水市高三上学期第一次月考化学试卷(解析版) 题型:选择题
室温下,在0.2mol/L Al2(SO4)3溶液中,逐滴加入1.0mol/L NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的是
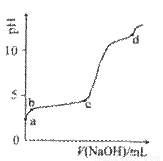
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:Al3+ + 3OH- Al(OH)3
Al(OH)3
B.a-b段,溶液pH增大,Al3+浓度不变
C.b-c段,加入的OH-主要用于生成Al(OH)3沉淀
D.d点时,Al(OH)3沉淀开始溶解
查看答案和解析>>
科目:高中化学 来源:2015届河北省衡水市高三上学期第一次月考化学试卷(解析版) 题型:选择题
向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸。下列离子方程式与事实不相符的是
A.OH―+CO32―+2H+→HCO3―+H2O B.2OH―+CO32―+3H+→HCO3―+2H2O
C.2OH―+CO32―+4H+→CO2↑+3H2O D.OH―+CO32―+3H+→CO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源:2015届河北省石家庄市五校联考高三上学期第一次月考化学试卷(解析版) 题型:填空题
(10分)某无色溶液,由 、
、 、
、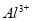 、
、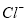 、
、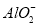 、
、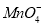 、
、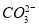 、
、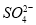 中的若干离子组成,将溶液平均分为两份置于两支试管:
中的若干离子组成,将溶液平均分为两份置于两支试管:
①取其中一支试管,加入过量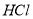 。有气体生成,并得到溶液;
。有气体生成,并得到溶液;
②在①所得溶液中加入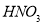 酸化的
酸化的 ,出现白色沉淀;
,出现白色沉淀;
③取另一支试管,先加入过量的HCl酸化,再加入过量的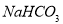 溶液,有气体生成同时析出白色沉淀甲,甲的质量为
溶液,有气体生成同时析出白色沉淀甲,甲的质量为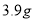 ;
;
④在③所得溶液中加入过量的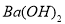 溶液,有白色沉淀乙析出。
溶液,有白色沉淀乙析出。
根据上述实验完成下列问题:
(1)溶液中一定不存在的离子是____________。
(2)一定存在的离子是________________________。
(3)判断沉淀乙成分的方法是____________________________________。
(4)写出有关反应的离子方程式
实验①:________________________________;____________________________;
(5)通过实验③可知溶液中存在的离子为________________________,原溶液中该离子的物质的量为____________。
查看答案和解析>>
科目:高中化学 来源:2015届江西省红色六校高三第一次联考化学试卷(解析版) 题型:填空题
(8分)已知A、B、C、D、E、F、G都是中学化学常见的物质,下图中A为淡黄色固体,
B、C为溶液,D、G为无色气体,E、F为白色沉淀。
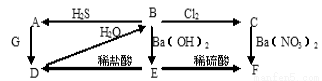
①写出B→C的离子方程式
②写出D和G反应的化学方程式
③写出过量的D通入Ba(OH)2溶液中的离子方程式
④从上图出现的物质中选出反应物,写出一个置换反应,以验证氯元素原子的氧化性比硫元素原子的氧化性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com