
【题目】
(1)某液体化合物X2Y4,常用做火箭燃料。16g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g)==X2(g)+2Y2O(l)。冷却后标准状况下测得生成物的体积为11.2 L,其密度为1.25 g·L-1,则:
①反应前O2的体积V(O2)为________。
②X2的摩尔质量为________________。
③Y元素的名称是________________。
(2)取1.43 g Na2CO3·xH2O溶于水配成50mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,共消耗盐酸20.0mL,并收集到112mLCO2(标准状况下)。
①稀盐酸物质的量浓度为________________mol·L-1
②Na2CO3·xH2O的摩尔质量为__________ g·mol-1
③x=________
【答案】11.2L 28 g·mol-1 氢元素 0.5 mol·L-1 286 g·mol-1 10
【解析】
(1)X元素形成的气体单质标准状况下的密度为1.25g/L,X2的摩尔质量为1.25g/L×22.4L/mol=28g/mol,则反应后的气体X2为N2,11.2L氮气的物质的量为0.5mol。
(2)根据反应方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑计算。
(1)①由反应方程式知,N2和氧气的物质的量之比为1:1,所以生成N2的体积等于消耗氧气的体积为11.2L;
②X元素形成的气体单质标准状况下的密度为1.25g/L,X2的摩尔质量为1.25g/L×22.4L/mol=28g/mol;
③根据氮气和N2Y4的关系式可知,反应N2Y4的物质的量为0.5mol,则M(N2Y4)=![]() 32g/mol,N元素的相对原子质量是14,所以Y的相对原子质量是1,Y为氢元素;
32g/mol,N元素的相对原子质量是14,所以Y的相对原子质量是1,Y为氢元素;
(2)112mLCO2(标准状况下)的物质的量是![]() =0.005mol;设HCl的物质的量为xmol,Na2CO3的物质的量为ymol;
=0.005mol;设HCl的物质的量为xmol,Na2CO3的物质的量为ymol;
Na2CO3+2HCl=2NaCl+H2O+CO2↑
1 2 1
y x 0.005
![]() ,x=0.01mol,y=0.005mol,
,x=0.01mol,y=0.005mol,
①稀盐酸物质的量浓度为![]() 0.5 mol·L-1mol·L-1
0.5 mol·L-1mol·L-1
②Na2CO3·xH2O的摩尔质量为![]() 286g·mol-1
286g·mol-1
③106+18x=286,x=10。


科目:高中化学 来源: 题型:
【题目】氯及其化合物的用途广泛,例如:“84”消毒液的有效成分是次氯酸钠,漂白精的有效成分是次氯酸钙,洁厕剂的有效成分是盐酸。已知酸性: H2CO3>HClO>HCO3-。下列有关说法正确的( )
A. “84”消毒液与洁厕剂混合使用,能增强漂白或去污效果
B. 工业上制取漂白粉往往是向澄清石灰水中通入足量氯气
C. 可设计实验装置,用电解饱和食盐水的方法制备次氯酸钠溶液
D. 向“84”消毒液中通入少量CO2,反应的化学方程式为2NaClO+CO2+H2O==Na2CO3+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4 kJ·mol-1。在恒容密闭容器内,投入2mol N2和6mol H2发生反应,当反应达到平衡状态时,下列说法不正确的是
2NH3(g) △H=-92.4 kJ·mol-1。在恒容密闭容器内,投入2mol N2和6mol H2发生反应,当反应达到平衡状态时,下列说法不正确的是
A. 当其他条件不变的情况下,升高温度,原有的平衡被破坏,逆反应速率增大,正反应速率减小
B. 一定存在2v(H2)正=3 v(N2)逆
C. 反应过程中可能放出92.4 kJ的热量
D. 容器内混合气体的平均相对分子质量不再发生变化时,说明反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某A在一定温度下有分解反应A(s) =B(s) + C(g) + 4D(g) 若测得生成的气体的质量是同温同压下相同体积氢气质量的10倍,且当所成气体在标准状况下的体积为22.4L时,所得B的质量为30.4g则A的摩尔质量是( )
A.130.4B.50.4C.182.4D.252
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一:制取氯酸钾和氯水
利用如图所示的实验装置进行实验。
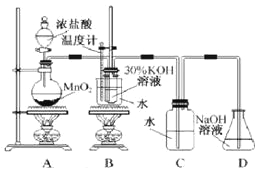
(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有__。
(2)若对调B和C装置的位置,__(填“能”或“不能”)提高B中氯酸钾的产率。
实验二:氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
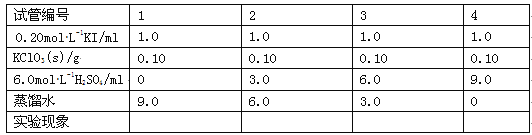
①系列a实验的实验目的是__。
②设计1号试管实验的作用是__。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为__。
实验三:测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用如图装置,加热15.0ml饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是__。(不考虑实验装置及操作失误导致不可行的原因)
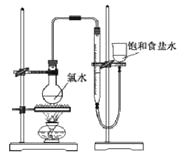
(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):__。
资料:i.次氯酸会破坏酸碱指示剂;
ii.次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】商代炼铜时,所用的矿物原料主要是孔雀石,主要燃料是木炭,在温度1000℃左右冶炼,可能涉及的反应有:
①Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O;
2CuO+CO2↑+H2O;
②2CuO+C![]() 2Cu+CO2↑;
2Cu+CO2↑;
③CuO+CO![]() Cu+CO2;
Cu+CO2;
④CO2+C![]() 2CO。
2CO。
(1)从四种基本反应类型来看,①②④的反应类型分别为①___________,②___________,④___________。
(2)反应③中,____________发生氧化反应,__________发生还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用如图装置所示方法制备氯气:
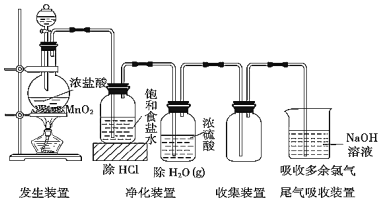
(1)1molMnO2和4mol浓盐酸制得的氯气的产量往往远低于1mol,原因可能是______
(2)实验结束后,取少量尾气吸收装置中所得溶液,滴加硫酸溶液有单质生成,反应的离子方程式是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知由金属钠制得氧化钠,可用多种方法:a.4Na+O2===2Na2O,b.4Na+CO2===2Na2O+C,c.2NaNO2+6Na===4Na2O+N2↑。
①在上述三种方法中,最好的方法是________(填序号),原因是________________。
②上述反应c中NaNO2作________剂,当有1 mol NaNO2反应时,电子转移的数目是________________________________________________________________________。
(2)现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如下。回答下列问题(注:Na2O2可以与H2O、CO2反应):
①装置Ⅳ中盛放的药品是________,其作用是____________________________。


②若规定气体的气流方向从左到右,则组合实验装置时各仪器接口的标号字母(a、b……)顺序:空气进入________,________接________,________接________,________接________。
③装置Ⅱ的作用____________________________________________________。
④操作中通空气和加热的顺序为________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二苯基乙二酮常用作医药中间体及紫外线固化剂,可由二苯基羟乙酮氧化制得,反应的化学方程式及装置图(部分装置省略)如图:
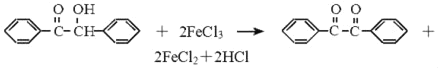
在反应装置中,加入原料及溶剂,搅拌下加热回流。反应结束后加热煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶 液重结晶提纯。重结晶过程:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
请回答下列问题:
(1)写出装置图中玻璃仪器的名称:b_____。
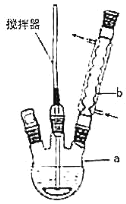
(2)趁热过滤后,滤液冷却结晶。一般情况下,下列哪些因素有利于得到较大的晶体:_____。
A.缓慢冷却溶液 B.溶液浓度较高 C.溶质溶解度较小 D.缓慢蒸发溶剂
如果溶液中发生过饱和现象,可采用_____等方法促进晶体析出。
(3)抽滤所用的滤纸应略_____(填“大于”或“小于”)布氏漏斗内径,将全部小孔盖住。 烧杯中的二苯基乙二酮晶体转入布氏漏斗时,杯壁上往往还粘有少量晶体,需选用液体将杯壁上的晶体冲洗下来后转入布氏漏斗,下列液体最合适的是_____。
A.无水乙醇 B.饱和NaCl溶液 C.70%乙醇水溶液 D.滤液
(4)抽滤过程中要及时观察吸滤瓶内液面高度,当快达到支管口位置时应进行的操作为_____。
(5)上述重结晶过程中的哪一步操作除去了不溶性杂质:_____。
(6)某同学采用薄层色谱(原理和操作与纸层析类同)跟踪反应进程,分别在反应开始、回流15min、30min、45min和60min时,用毛细管取样、点样、薄层色谱展开后的斑点如图所示。该实验条件下比较合适的回流时间是_____。
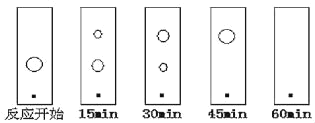
A.15min B.30min C.45min D.60min
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com