
| A. | 1molCl2溶于水反应,反应转移电子数为nA | |
| B. | 56g晶体硅中含有硅分子数为2nA | |
| C. | 1 mol Cu和足量稀硝酸反应产生nA个NO分子 | |
| D. | 标准状况下,1.12 L NO与1.12 L O2的混合物中含有的原子数为0.2nA |
分析 A、氯气与水的反应为歧化反应;
B、晶体硅是原子晶体;
C、根据得失电子数守恒来分析;
D、标准状况下,1.12 L NO与1.12 L O2的物质的量均为0.05mol,根据反应后原子个数守恒来分析.
解答 解:A、氯气与水的反应为歧化反应,故1mol氯气溶于水后转移的电子数小于nA个,故A错误;
B、晶体硅是原子晶体,故在晶体硅中无硅分子,故B错误;
C、根据电子守恒计算,1molCu失2mole-,HNO3还原为NO,只生成$\frac{2}{3}$molNO,因此不应产生nA个NO分子,故C错误;
D、标准状况下,1.12 L NO与1.12 L O2的物质的量均为0.05mol,而NO和氧气均为双原子分子,故0.05molNO和0.05mol氧气中均含0.1mol原子,而两者混合后发生反应生成二氧化氮,但由于反应过程中原子个数守恒,故混合后原子个数仍为0.2nA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
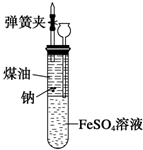 有人设计出一种在隔绝空气条件下让钠与FeSO4溶液反应的方法以验证反应实质.实验时,往100mL大试管中先加40mL煤油,取3粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入用煮过的蒸馏水配制的FeSO4溶液使煤油的液面至胶塞,并夹紧弹簧夹(如图).仔细观察,回答下列问题:
有人设计出一种在隔绝空气条件下让钠与FeSO4溶液反应的方法以验证反应实质.实验时,往100mL大试管中先加40mL煤油,取3粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入用煮过的蒸馏水配制的FeSO4溶液使煤油的液面至胶塞,并夹紧弹簧夹(如图).仔细观察,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L水含有NA个水分子 | |
| B. | 氧气和臭氧的混合物32 g中含有NA个氧原子 | |
| C. | 0.1mol Na2O2与水反应时转移0.1NA个电子 | |
| D. | 11.2 L氯气中含有NA个氯原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 与
与 B.
B. 与
与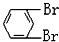 C.
C. 与
与 D.
D. 与
与 E.ClC(CH3)3与(CH3)2CHCH2Cl F.
E.ClC(CH3)3与(CH3)2CHCH2Cl F.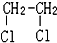 与CH3-CH2Cl
与CH3-CH2Cl 由一种单体脱水缩聚而成的,该单体的键线式为
由一种单体脱水缩聚而成的,该单体的键线式为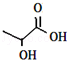
 )滴入Na2CO3溶液中,生成的有机物的结构简式是:
)滴入Na2CO3溶液中,生成的有机物的结构简式是:
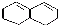 在较高温度下和Br2按物质的量之比1:1发生1,4-加成反应的化学方程式
在较高温度下和Br2按物质的量之比1:1发生1,4-加成反应的化学方程式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气既能用浓硫酸干燥也能用无水CaCl2干燥 | |
| B. | NH3是电解质,所以氨水能导电 | |
| C. |  用水吸收NH3用如图装置可防止倒吸 | |
| D. | NH3可以使干燥的红色石蕊试纸变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳和氮气 | B. | 二氧化碳和二氧化氮 | ||
| C. | 二氧化碳和氧气 | D. | 氮气和氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
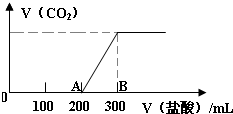 向100mL 3mol/L的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的PH>7.
向100mL 3mol/L的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的PH>7.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com