

| A. | 具有4个官能团,氯原子、苯基、羟基和羧基 | |
| B. | 具有羧基,能与醇类物质发生酯化反应 | |
| C. | 具有酚羟基,所以能与NaHCO3溶液反应生成CO2 | |
| D. | 具有氯原子,在氢氧化钠醇溶液中加热,可发生消去反应 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1Na2CO3溶液:c(Na+)>c(CO${\;}_{3}^{2-}$)>c(HCO${\;}_{3}^{-}$)>c(OH-) | |
| B. | 0.01 mol•L-1CH3COOH溶液,水电离出的c(H+)=10-12mol•L-1 | |
| C. | 0.2 mol•L-1NaClO溶液:c(Na+)═c(ClO-)+c(Cl-)+c(HClO) | |
| D. | pH相同的NH4Cl、(NH4)2SO4溶液:c(NH4Cl)>c[(NH4)2SO4] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
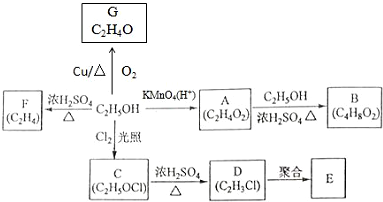
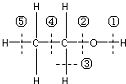
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
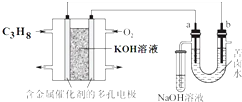 用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )
用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )| A. | 电池工作时,负极反应式为:C3H8+26OH--20e-═3CO${\;}_{3}^{2-}$+17H2O | |
| B. | 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者 | |
| C. | 电解时,电子流动的路径是:负极→外电路→阴极→溶液→阳极→正极 | |
| D. | 忽略能量损耗,当电池中消耗 0.16 g O2时,a极周围会产生0.71 g Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极产生的Cl2进入阳极室 | |
| B. | 用水可以一次性鉴别硝基苯、甲苯、冰醋酸三种物质 | |
| C. | 制硫酸和氢氧化钠:用如图所示装置 (注:b为阴离子交换膜、c为阳离子交换膜) (注:b为阴离子交换膜、c为阳离子交换膜) | |
| D. | 乙醛的氧化:在试管里加入10%的NaOH溶液2 mL,滴入2%的CuSO4溶液4滴~6滴,振荡后加入乙醛溶液0.5 mL,加热至沸腾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
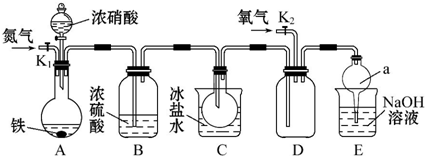
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量 | B. | 密度 | C. | 原子数 | D. | 物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com