
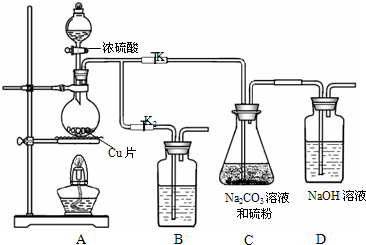
在C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O反应中,________是氧化剂,________是还原剂,________元素被还原,________是氧化产物,浓H2SO4表现的性质是________.
CO2↑+2SO2↑+2H2O反应中,________是氧化剂,________是还原剂,________元素被还原,________是氧化产物,浓H2SO4表现的性质是________.
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| 编 号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 | 充电 |
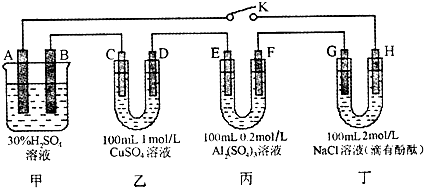
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、③④ | B、①② | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源:湖南省宜章一中2009-2010学年高一上学期期中考试化学试题 题型:022
在
C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O反应中,(1)在上述化学方程式中标明电子转移的方向和数目.(2)
氧化剂是________,氧化产物是________(填化学式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com