
【题目】如图所示,将一瓶充满NO2气体的试管倒扣在水槽中,气体颜色由____逐渐变为____色,试管内的液面会逐渐_____________;当反应停止后向试管中缓慢通入氧气,气体颜色又由______色逐渐变为______色,之后又变为______色,试管内的液面会____________。用化学方程式表示试管中发生的化学反应_____________,____________。
【答案】红棕色无色上升无色红棕色无色继续上升3NO2+ H2O = 2HNO3+ NO4NO + 3O2+ 2H2O = 4HNO3
【解析】
将一瓶充满NO2气体的试管倒扣在水槽中,二氧化氮与水反应生成一氧化氮,3NO2+ H2O = 2HNO3+ NO,气体颜色由红棕色逐渐变为无色,试管内的液面会逐渐上升;当反应停止后向试管中缓慢通入氧气,一氧化氮与氧气反应生成二氧化氮,气体颜色又由无色逐渐变为红棕色,之后又变为无色,如此反复,当恰好完全反应时,发生4NO + 3O2+ 2H2O = 4HNO3,因此试管内的液面会继续上升,故答案为:红棕色;无;上升;无;红棕;无;上升;3NO2+ H2O = 2HNO3+ NO;4NO + 3O2+ 2H2O = 4HNO3。


科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.铝与稀硫酸反应:Al+2H+= Al 3++H2↑
B.碳酸钙与稀盐酸的反应:CO32-+2H+=CO2+H2O
C.氢氧化铁与盐酸的反应:H++OH-=H2O
D.三氯化铁腐蚀印刷线路板:2Fe3++Cu=2Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.78 g Na2O2固体中含有的阴离子数为NA(相对原子质量Na:23 O:16)
B.标准状况下,11.2 L乙烯含有的共价键数目为3NA
C.在0 ℃、101 kPa时,金属钠从水中置换出22.4 L H2,发生转移的电子数为2NA
D.在25 ℃时,pH=13的NaOH溶液中含有的OH-数约为6.02×1022
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的正确判断的是
A.在pH= 12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存
B.在pH =0的溶液中,Na+、NO3-、SO32-、K+可以常量共存
C.由0.l mol/L一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH![]() B++OH-
B++OH-
D.pH =2的一元酸和pH =12的一元强碱等体积混后溶液一定存在:c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释过程或事实的方程式不正确的是( )
A. 氨气遇浓盐酸产生白烟:NH3+HCl═NH4Cl
B. NH4Cl与NaOH溶液反应的离子方程式:NH4++OH﹣═NH3↑+H2O
C. SO2使Br2水褪色:SO2 +Br2+2H2O═2HBr+H2SO4
D. SO2溶于水:SO2+2H2O![]() H2SO3
H2SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)元素的第一电离能:N________O(填“>”或“<”)。
(2)基态Fe2+的电子排布式为___________________________。
(3)在N、Mg、Al、Si四种元素中,有一种元素的电离能数据如下:
电离能 | I1 | I2 | I3 | I4 | … |
In/kJ·mol-1 | 578 | 1 817 | 2 745 | 11 575 | … |
则该元素的元素符号是________。
(4)NO![]() 的空间构型_____________________(用文字描述),SO
的空间构型_____________________(用文字描述),SO![]() 中硫原子的杂化方式为________________________。
中硫原子的杂化方式为________________________。
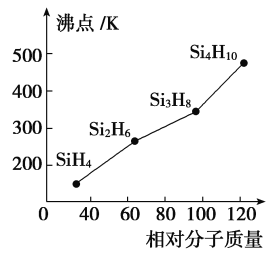
(5)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是_______________________。
(6)金属铜原子的堆积方式为面心立方最密堆积,铜的原子半径为r nm,则铜晶胞的体积表达式为________ cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟在自然界中常以CaF2的形式存在。
(1)下列有关CaF2的表述正确的是________。
a.Ca2+与F-间仅存在静电吸引作用
b.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
c.阴阳离子比为2∶1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是________(用离子方程式表示)。已知AlF![]() 在溶液中可稳定存在。
在溶液中可稳定存在。
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为________,其中氧原子的杂化方式为________。
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)===2ClF3(g) ΔH=-313 kJ·mol-1,F—F键的键能为159 kJ·mol-1,Cl—Cl键的键能为242 kJ·mol-1,则ClF3中Cl—F键的平均键能为________kJ·mol-1。ClF3的熔、沸点比BrF3的________(填“高”或“低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com