
实验室可以用饱和FeCl3溶液制备Fe(OH)3胶体.
(1)写出制备Fe(OH)3胶体的化学方程式
(2)取烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加稀盐酸至过量,边滴边振荡,可以看到的现象是
 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源:2015-2016学年福建省高二上学期半期考试化学试卷(解析版) 题型:实验题
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。

发生的反应如下:
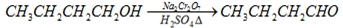
反应物和产物的相关数据如下:
沸点/℃ | 密度(g.cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.5 | 0.8107 | 微溶 |
实验步骤如下:
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。
②在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分。
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。
回答下列问题:
(1)B仪器的名称是 ,D仪器的名称是 。
(2)沸石的作用是 。
(3)将正丁醛粗产品置于分液漏斗中分液时,水在 层(填“上”或“下” )
(4)反应温度应保持在90~95℃,其原因是 。
(5)本实验中,正丁醛的产率为 %。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省三门峡市高二上学期期中测试化学试卷(解析版) 题型:选择题
如图曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
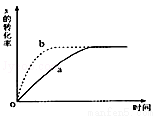
A.升高温度 B.加大X的投入量
C.缩小体积 D.减小N的投入量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省许昌、襄城、长葛三校高一上期中测试化学试卷(解析版) 题型:选择题
“钴酞菁(直径为1.5×10-9 m)”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似,我国科学家在世界上第一次为“钴酞菁”分子恢复了磁性。下列说法不正确的是
A.“钴酞菁”分子所形成的分散系具有丁达尔效应
B.“钴酞菁”分子既能透过滤纸,也能透过半透膜
C.此项工作可以用来改变分子的某些物理性质
D.将磁性物质制成胶体粒子作为药物的载体,可在磁场作用下送到病灶处。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省宜宾市高二上学期期中测试化学试卷(解析版) 题型:选择题
中学化学教材中有大量数据,下列是某同学对数据利用情况,正确的是
A.利用焓变的数据或熵变的数据一定都能单独判断反应是否能自发进行
B.利用反应热数据的大小判断不同反应的反应速率的大小
C.利用沸点数据推测将一些液体混合物分离开来的可能性
D.利用溶液的pH与7的大小关系,判断PH=6.8的溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上学期11月阶段性测试化学试卷(解析版) 题型:选择题
四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2 和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为
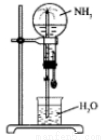
A.①>②>③>④ B.①=②=③=④
C.①=②=③>④ D.①=②>③>④
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第二次月考化学试卷(解析版) 题型:填空题
硅是信息产业、太阳能电池光电转化的基础材料。锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意如下:

(1)硅元素位于元素周期表的第______________周期____________族。
(2)已知反应Ⅰ得到的粗硅中含有SiC,其中Si和SiC的物质的量之比为2∶1。写出制造粗硅时的反应方程式 。SiC熔融时不导电,工业上常用作耐火和高温炉的材料,由此推知,它属于____________晶体。
(3)因为SiCl4遇水剧烈水解生成SiO2和一种酸,所以整个制备过程必须严格控制无水条件。在干燥Cl2时,从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入到浓H2SO4中。冷却的作用是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市兖州区高一上学期期中测试化学试卷(解析版) 题型:实验题
碘是人体不可缺少的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是: 在溶液中 KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)用双线桥表示该反应中电子转移的方向和数目
该反应中还原产物与氧化产物的物质的量比是__________,0.2mol KIO3参加反应时转移电子__________mol
(2)实验结束后分离I2和K2SO4溶液所用的试剂是________
A.CCl4 B.酒精 C.Na2SO4溶液 D.食盐水
所用的分离方法是 ,所用主要玻璃仪器是
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制1 mol/L的稀硫酸溶液480mL,需用18mol/L浓H2SO4 mL,配制中需要用到的主要玻璃仪器是(填序号) .
A 100mL量筒 B 托盘天平
C 玻璃棒 D 100mL容量瓶
E 50mL 量筒 F 胶头滴管 G 烧杯 H 500mL容量瓶
(4)下面操作造成所配稀硫酸溶液浓度偏高的是___________
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com