
某学生设计了如下4个实验方案,用以检验淀粉的水解程度,其中操作和结论均正确的是( )
A.淀粉液![]() 水解液
水解液![]() 中性液
中性液![]() 溶液变蓝,结论:淀粉尚未水解
溶液变蓝,结论:淀粉尚未水解
B.淀粉液![]() 水解液
水解液![]() 碱性液
碱性液![]() 生成银镜,结论:淀粉水解完全
生成银镜,结论:淀粉水解完全
C.淀粉液![]() 水解液
水解液![]() 无银镜现象,结论:淀粉尚未水解
无银镜现象,结论:淀粉尚未水解
D.淀粉液![]() 水解液
水解液![]()
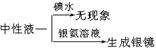 ,结论:淀粉水解完全
,结论:淀粉水解完全
科目:高中化学 来源: 题型:
 (1)称量所需要的仪器是
(1)称量所需要的仪器是| bV |
| 200 |
| bV |
| 200 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.淀粉液![]() 水解液
水解液![]() 中性液
中性液![]() 溶液变蓝,结论:淀粉尚未水解
溶液变蓝,结论:淀粉尚未水解
B.淀粉液![]() 水解液
水解液![]() 碱性液
碱性液![]() 生成银镜,结论:淀粉水解完全
生成银镜,结论:淀粉水解完全
C.淀粉液![]() 水解液
水解液![]() 无银镜现象,结论:淀粉尚未水解
无银镜现象,结论:淀粉尚未水解
D.淀粉液![]() 水解液
水解液![]()
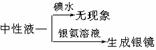 ,结论:淀粉水解完全
,结论:淀粉水解完全
查看答案和解析>>
科目:高中化学 来源: 题型:
为测定碳酸钠的质量分数(设含杂质碳酸氢钠),某学生设计了如下两个实验方案,请回答每个方案中的问题。
 [方案Ⅰ] 重量法:
[方案Ⅰ] 重量法:
| |||
|
(1)称量所需要的仪器是 。
(2)样品放在 仪器中灼烧。
a.蒸发皿 b.烧杯 c.坩埚
(3)实验中操作A的名称为 。
(4)如果灼烧后的样品放在空气中冷却,会造成实验结果 (填“偏大”、“偏小”或“不变”)。
(5)样品碳酸钠的质量分数 。已知该样品碳酸钠的质量分数为0.913,则本次实验的相对误差为 。
[方案II] 滴定法:①称取样品 M g;②用amol/L 过量盐酸VmL在烧杯中溶解样品,并加水稀释配成100mL溶液;③取溶解后的溶液20.00mL,用bmol/L NaOH溶液滴定,恰好用去V,mL;④重复③的操作2~3次。
(6)配成上述溶液所需要的容器的名称是 。滴定中还需要的试剂是 。
(7)操作④的目的是 。
(8)滴定测得的过量盐酸中含HCl的总物质的量的表达式为 。
(9)下列操作会使过量盐酸中含HCl测定值偏小的是 。
a.盛放氢氧化钠的滴定管只用蒸馏水洗涤
b.滴定过程中有液体溅出
c.滴定中用蒸馏水冲洗锥形瓶内壁
(10)综上所述,你认为2个方案中,较好的方案是 。
查看答案和解析>>
科目:高中化学 来源:2010年上海市卢湾区高考模拟考试 题型:实验题
为测定碳酸钠的质量分数(设含杂质碳酸氢钠),某学生设计了如下两个实验方案,请回答每个方案中的问题。
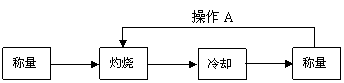 [方案Ⅰ] 重量法:
[方案Ⅰ] 重量法:
|
|||
|
(1)称量所需要的仪器是 。
(2)样品放在 仪器中灼烧。
a.蒸发皿 b.烧杯 c.坩埚
(3)实验中操作A的名称为 。
(4)如果灼烧后的样品放在空气中冷却,会造成实验结果 (填“偏大”、“偏小”或“不变”)。
(5)样品碳酸钠的质量分数 。已知该样品碳酸钠的质量分数为0.913,则本次实验的相对误差为 。
[方案II] 滴定法:①称取样品 M g;②用amol/L 过量盐酸VmL在烧杯中溶解样品,并加水稀释配成100mL溶液;③取溶解后的溶液20.00mL,用bmol/L NaOH溶液滴定,恰好用去V,mL;④重复③的操作2~3次。
(6)配成上述溶液所需要的容器的名称是 。滴定中还需要的试剂是 。
(7)操作④的目的是 。
(8)滴定测得的过量盐酸中含HCl的总物质的量的表达式为 。
(9)下列操作会使过量盐酸中含HCl测定值偏小的是 。
a.盛放氢氧化钠的滴定管只用蒸馏水洗涤
b.滴定过程中有液体溅出
c.滴定中用蒸馏水冲洗锥形瓶内壁
(10)综上所述,你认为2个方案中,较好的方案是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com