
【题目】化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25℃时,反应进行l0 min,溶液的pH由7变为l 2。
①N2的结构式为
②上述反应的离子方程式为 ,其平均反应速率v(NO3-)为 mol·L-1·min-1。
③还原过程中可生成中间产物NO2-,写出2种促进NO2-水解的方法 。
(2)电化学降解NO3-的原理如下图所示。
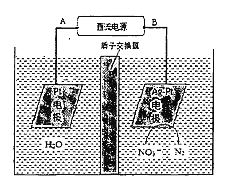
①电源正极为 (填“A”或“B”),阴极反应式为:
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为 g。
【答案】(1)①N≡N 2NO3-+5H2![]() N2+2OH-+4H2O 0.001mol/(L·min)
N2+2OH-+4H2O 0.001mol/(L·min)
③加酸,升高温度,加水
(2)A, 2NO3-+6H2O+10e-=N2+12OH- ②14.4
【解析】
试题分析:(1) ②废水不应显酸性(HNO3易挥发),而是中性或碱性,所以O2-在水中以H2O或OH-形式存在,有题意也可看出生成OH-(溶液pH由7变为12),依据氧化还原反应规律可配平:

pH=12![]() c(H+)=1×10-12mol·L-1
c(H+)=1×10-12mol·L-1
![]() c(OH-)=
c(OH-)= ![]() 1×10-2mol·L-1
1×10-2mol·L-1
υ(NO3-)=υ(OH-)= 1×10-10mol·L-1 /10min= 0.001mol·L-1·min-1
③由方程式知NO2-+H2O![]() HNO2+OH- △H>0 ,加热,加酸均可均可使平衡正向移动,促进NO2-转化。
HNO2+OH- △H>0 ,加热,加酸均可均可使平衡正向移动,促进NO2-转化。
(2)①2![]() O3-+10e-→
O3-+10e-→![]() +6O2,所以B极为电源负极,A极为电源正极。
+6O2,所以B极为电源负极,A极为电源正极。
O2-+H2O=2OH-,可以写出阴极反应式:2NO3-+6H2O+10e- = N2↑+12OH-
② 左(+)阳极:4H2O(OH-)-4e-=4H++O2↑+2H2O
右(- )阴极:2NO3-+6H2O+10e- = N2↑+12OH-
10 e-![]() O2(左)- 1N2(右)-10H+
O2(左)- 1N2(右)-10H+
10mol ![]() mol 1mol 10mol
mol 1mol 10mol
2mol 0.5mol 0.2mol 2mol
由于阴阳极之间被质子交换膜隔开,左侧电解产生的H+会穿过质子交换膜进入右侧,所以:
△m左=m(O2)+m(H+)=0.5mol×32g·mol-1+2mol×1g·mol-1=18g
△m右= m(N2)-m(H+)=0.2mol×28g·mol-1-2mol×1g·mol-1=3.6g
△m左-△m右=18g-3.6g = 14.4g


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)H2(g)+I2(g).若[HI]由0.1molL﹣1降到0.07molL﹣1时,需要15s,那么[HI]由0.07molL﹣1降到0.05molL﹣1时,所需反应的时间为( )
A.等于5 s
B.等于10 s
C.大于10 s
D.小于10 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列比较中正确的是( )
A.离子还原性:S2->Cl->Br->I-
B.氧化性:F2>Cl2>Br2>S
C.酸性:H2SO4>HClO4>H3PO4
D.非金属性:F>Cl>S>O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种物质中 ①Ne ②H2O ③NH3④KOH ⑤Na2O(填写序号):只存在共价键的是 ,只存在离子键的是 ,既存在共价键又存在离子键的是 ,不存在化学键的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传统的冰箱制冷剂“氟利昂”( CCl2F2)泄漏后台破坏臭氧层.其反应过程可表示为:O3﹣→O+O2;Cl+O3→ClO+O2;ClO+O→Cl+O2 , 总反应为2O3→3O2 . 则上述臭氧变成氧气的反应过程中,Cl原子的作用是( )
A.氧化剂
B.还原剂
C.催化剂
D.稳定剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A.原子晶体中一定不存在化学键B.离子晶体中只存在离子键
C.在共价化合物中一定有共价键D.非金属原子间只能形成共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:
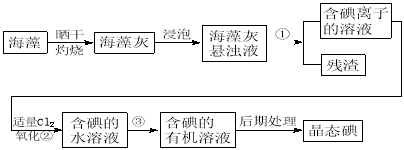
⑴ 在提取碘的过程中有关实验的操作名称:① ,③ ;写出过程②中有关反应的化学方程式: 。
⑵提取碘的过程中,可供选择的有机试剂是 。
A.酒精 B.苯 C.乙酸 D.四氯化碳
⑶为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是 。
⑷从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏。指出如图所示实验装置中的错误之处: ; ; 。
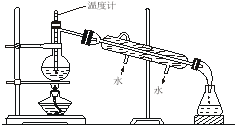
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com