
【题目】KBBF 品体[氟代硼铍酸钾(KBe2BO3F2)]是用于制造深紫外激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)基态F原子中能量最高的电子其电子云轮廓图为_______形;基态K原子的核外电子排布式为______。
(2)氮与氧均为第二周期元素,请判断N元素与O元素的第一电离能I1(N)_____I1(O)(填"大于"“小于”或“等于”),原因是_____________。
(3)H3BO3是一种一元弱酸,可与NaOH 溶液反应生成Na[B(OH)4],在硼酸和B(OH)4—中B原子的杂化方式分别为________。
(4)BF3是一种 _________分子(填写“极性”或“非极性”),BF3分子的空间构型为____________,与BF3互为等电子体的分子或离子有________(写出一种即可)。
(5)周期表中,某些主族元素的左上或右下元素的性质是相似的,被称为对角线规则。写出Be元素最高价氧化物的水化物与NaOH溶液反应的离子方程式________。
【答案】哑铃 [Ar]4s1 大于 氮原子价层2p能级处于较稳定的半充满状态,难于失去电子 sp2 sp3 非极性 SO3 ![]()
【解析】
(1)基态F原子中,能量最高的电子为p电子,电子云轮廓图为纺锤形或无柄哑铃形,基态K原子的核外电子排布式为[Ar]4s1;
(2)根据洪特规则,当电子亚层中电子处于半充满、全充满和全空状态时,最稳定,氮原子价层2p能级处于较稳定的半充满状态,难于失去电子,因此I1(N)> I1(O);
(3)根据VSEPR理论和杂化轨道原理,硼酸的中心原子B的杂化方式为sp2杂化,而B(OH)4—中的B原子由于接收了O原子的一对孤对电子形成配位键,故采取sp3杂化;
(4)BF3的正电中心与负电中心重合,为非极性分子,BF3分子的空间构型为平面三角形,与BF3互为等电子体的分子或离子有SO3等;
(5)根据对角线规则,Be与Al元素的性质相似,Be元素最高价氧化物的水化物与NaOH溶液反应的离子方程式为![]() 。
。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:

下列叙述错误的是
A. X、Y和Z均能使溴水褪色
B. X和Z均能与NaHCO3溶液反应放出CO2
C. Y既能发生取代反应,也能发生加成反应
D. Y可作加聚反应单体,X可作缩聚反应单体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaHCO3和Na2O2的固体混合物x g在密闭容器中加热至250℃,充分反应后排出气体.将反应后的固体溶入水无气体放出,再逐滴加入盐酸,产生气体(标准状况)与所加盐酸体积之间的关系如图所示.下列说法错误的是( )
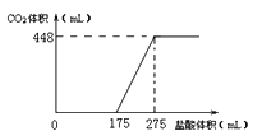
A.HCl的浓度0.2mol/L
B.反应后固体的成分为NaOH与Na2CO3
C.密闭容器中排出气体的成分为O2和H2O
D.x的数值为6.09
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用琥珀酸酐法制备了DEN人工抗原及抗体.如图是1,3﹣丁二烯合成琥珀酸酐的流程:
1,3丁二烯![]() C4H6Br2
C4H6Br2![]() A
A![]() B
B![]() C
C![]()

完成下列填空:
(1)写出反应试剂和反应条件.反应①______;反应②______.
(2)比1,3﹣丁二烯多一个C并且含1个甲基的同系物有______种.
(3)写出A和C的结构简式.A______;C______.
(4)写出B和C反应生成高分子化合物的化学方程式______.
(5)设计一条由1,3﹣丁二烯为原料制备![]() 的合成路线.(无机试剂可以任选)_____
的合成路线.(无机试剂可以任选)_____
(合成路线常用的表示方式为:A![]() B…
B…![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在高中阶段,安排了两种酯的制备实验:
乙酸乙酯的制备
乙酸丁酯[CH3COO(CH2)3CH3]的制备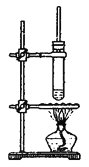
制备这两种酯所涉及的有关物质的物理性质见下表:
乙酸 | 乙醇 | 1—丁醇 | 乙酸乙酯 | 乙酸丁酯 | |
熔点(℃) | 16.6 | -117.3 | -89.5 | -83.6 | -73.5 |
沸点(℃) | 117.9 | 78.5 | 117 | 77.06 | 126.3 |
密度(g/cm3) | 1.05 | 0.79 | 0.81 | 0.90 | 0.88 |
水溶性 | 互溶 | 互溶 | 可溶 (9g/100克水) | 可溶 (8.5g/100克水) | 微溶 |
请回答下列问题:
(1)在乙酸乙酯的制备过程中,采用水浴加热的优点为_______________________;而乙酸丁酯的制备过程中未采用水浴加热的原因是______________。
(2)提纯时,乙酸乙酯一般采用______洗涤,而乙酸丁酯可先采用______、后采用______洗涤(均填编号)。
a.水 b.15%Na2CO3溶液 c.饱和Na2CO3溶液
(3)两种酯的提纯过程中都需用到的关键仪器是______________,在操作中要注意振荡洗涤后,静置分液前必须要有步骤,所制得的酯应从该仪器的________(填编号)。
a.下部流出 b.上口倒出 c.都可以
(4)在乙酸乙酯制备中,采用了乙醇量,下列说法不正确的是_______(填编号)。
a.乙醇比乙酸价廉 b.提高乙酸的转化率
c.提高乙醇的转化率 d.提高乙酸乙酯的产率
(5)在乙酸丁酯制备中,下列方法可提高1—丁醇利用率的是________(填编号)。
a.使用催化剂 b.加过量乙酸 c.不断移去产物 d.缩短反应时间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种镁氧电池如图所示,电极材料为金属镁和吸附氧气的活性炭,电解液为KOH浓溶液。下列说法不正确的是( )

A.电池总反应式为:2Mg+ O2+2H2O=2Mg(OH)2
B.正极反应式为:Mg-2e-=Mg2+
C.活性炭可以加快O2在电极上的反应速率
D.电子的移动方向由a经外电路到b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近在-100 ℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示。下列说法中不正确的是( )
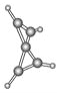
A. 该分子的分子式为C5H4
B. 该分子中碳原子的化学环境有2种
C. 该分子中的氢原子分布在两个相互垂直的平面上
D. 该分子中只有C—C键,没有![]() 键
键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是
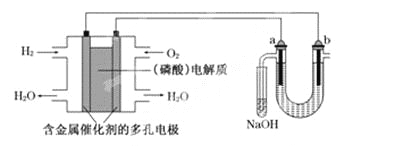
A. 电池工作时,正极反应式为: O2+2H2O+4e-===4OH-
B. 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者
C. 电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D. 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.04 g H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com