
| 元素 | A | B | C | D |
| 性质 结构 信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104s1, 有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“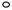 ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键。
”表示没有形成共价键的最外层电子,短线表示共价键。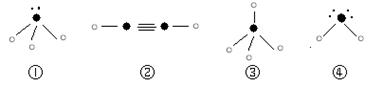
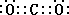 Fe2O3(s) + 3CO(g)
Fe2O3(s) + 3CO(g)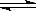 2Fe(s) + 3CO2(g) K=C3(CO2)/ C3(CO)(各1分)
2Fe(s) + 3CO2(g) K=C3(CO2)/ C3(CO)(各1分)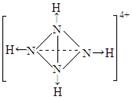 (2分)
(2分)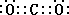 ,高温下D的氧化物还原赤铁矿的方程式为可逆反应,该反应的化学方程式Fe2O3(s) + 3CO(g)
,高温下D的氧化物还原赤铁矿的方程式为可逆反应,该反应的化学方程式Fe2O3(s) + 3CO(g)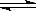 2Fe(s) + 3CO2(g) ; 该反应的平衡常数表达式K=C3(CO2)/ C3(CO) ;C原子核外电子排布为[Ar]3d104s1,有+1、+2两种常见化合价
2Fe(s) + 3CO2(g) ; 该反应的平衡常数表达式K=C3(CO2)/ C3(CO) ;C原子核外电子排布为[Ar]3d104s1,有+1、+2两种常见化合价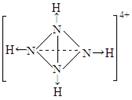


科目:高中化学 来源:不详 题型:填空题
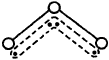
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
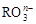 和I-发生反应的离子方程式为:
和I-发生反应的离子方程式为: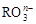 +6I-+6H+=R-+3I2+3H2O(R为主族元素)则:
+6I-+6H+=R-+3I2+3H2O(R为主族元素)则: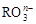 中R的化合价为 价,n值为 。
中R的化合价为 价,n值为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NF3是离子化合物 | B.NF3的还原性比NH3强 |
| C.NF3的氧化性比F2强 | D.NF3中的N呈+3价 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.与硅相比,金刚石的硬度大,熔点高 |
| B.HF、HCl、HBr、HI热稳定性依次减弱 |
| C.F2、Cl2、Br2、I2的沸点逐渐升高 |
| D.F2比O2更容易与H2反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


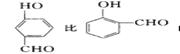 沸点 。(填高或低)
沸点 。(填高或低)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SiO2和CaO的熔化 | B.氧化钠和铁的熔化 |
| C.碘和干冰的气化 | D.晶体硅和晶体硫的熔化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若n=2,则分子的立体构型为V形 | B.若n=3,则分子的立体构型为三角锥形 |
| C.若n=4,则分子的立体构型为正四面体形 | D.以上说法都不正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com