
【题目】碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法错误的是
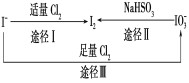
A. 用KI淀粉试纸和食醋无法检验加碘盐中是否含有碘
B. 足量Cl2能使湿润的KI淀粉试纸先变蓝后褪色,褪色的原因可能是:5Cl2+I2+6H2O = 2HIO3+10HCl
C. 由图可知氧化性的强弱顺序为Cl2>IO3->I2
D. 途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA
【答案】A
【解析】
A.加碘盐中含有KIO3,其在酸性条件下可被I-还原生成I2;
B.根据图示转化Ⅲ可知:足量的Cl2与I-反应生成NaIO3,氯气被还原为氯离子;
C.由途径I可知氧化性Cl2>I2,由途径Ⅱ可知氧化性I2<NaIO3,由途径Ⅲ可知氧化性Cl2>NaIO3;
D.根据转化关系2IO3-~I2~10e-计算判断.
A.加碘盐中含有KIO3,其在酸性条件下可被I-还原生成I2,故用淀粉-KI试纸和食醋检验加碘盐时淀粉-KI试纸会变蓝,故A错误;
B.根据图示转化Ⅲ可知:足量的Cl2与I-反应生成NaIO3,氯气被还原为氯离子,则足量Cl2能使湿润的KI淀粉试纸变白的原因可能是:5Cl2+I2+6H2O=2HIO3+10HCl,故B正确;
C.由途径I可知氧化性Cl2>I2,由途径Ⅱ可知氧化性I2<NaIO3,由途径Ⅲ可知氧化性Cl2>NaIO3,故氧化性的强弱顺序为Cl2>IO3->I2,故C正确;
D.根据转化关系2IO3-~I2~10e-可知,生成1 molI2反应中转移的电子数为10NA,故D正确;
故选:A。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应物的总键能与生成物的总键能之差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),该反应的反应热△H为 ( )
Si(s)+4HCl(g),该反应的反应热△H为 ( )
A. +412 kJ·mol-1 B. -412 kJ·mol-1
C. +236 kJ·mol-1 D. -236 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应的化学方程式为CO2+2Mg=C+2MgO,该反应属于:①化合反应 ②分解反应 ③置换反应 ④复分解反应 ⑤氧化还原反应 ⑥离子反应 ⑦非氧化还原反应
A.①③⑦B.②③⑥C.③⑤D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O![]() Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2 -e— + OH- = NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素的族序数之和是A元素族序数的2倍,B和C原子序数之和是A的四倍;则A、B、C分别为( )

A. Be、Na、AlB. B、Mg、Si
C. C、Al、PD. O、P、Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应4NH3+5O2![]() 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) (单位皆为molL-1min-1)表示,则下列式子中,正确的是( )
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) (单位皆为molL-1min-1)表示,则下列式子中,正确的是( )
A. 4v(NH3)=5 v(O2)B. 5 v(O2)=6 v(H2O)
C. 2v(NH3)=3 v(H2O)D. 4v(O2)=5 v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对三硫化四磷分子的结构研究表明,该分子中所有原子均以单键连接,且各原子的最外层均已达到8个电子的稳定结构。在一个三硫化四磷分子中含有的共价键的个数是 ( )
A. 19 B. 7 C. 9 D. 不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com