
(13分)I、煤炭中以FeS2形式存在的硫,在有水和空气及在脱硫微生物存在下发生生物氧化还原反应,有关反应的离子方程式依次为:
①2FeS2+7O2+2H2O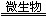 4H++2Fe2++4SO42- ;
4H++2Fe2++4SO42- ;
②Fe2++O2+H+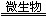 Fe3++____________;
Fe3++____________;
③FeS2+2Fe3+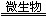 3Fe2++2S;
3Fe2++2S;
④2S+3O2+2H2O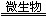 4H++2SO42-。
4H++2SO42-。
已知:FeS2中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②离子方程式配平并补充完整
(2)反应③的还原剂是__________________。
(3)观察上述反应,硫元素最终转化为____________从煤炭中分离出来
II、在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是_____________________________ 。在上述蓝色溶液中,继续滴加足量的NaClO溶液,蓝色逐渐消失,有关反应的离子方程式是_______________________ _。(提示:碘元素被氧化成IO3—)从以上实验可知,ClO—、I2、IO3—的氧化性由强到弱的顺序是 。
III、工业上用黄铜矿( CuFeS2)冶炼铜,副产品中也有SO2 ,冶炼铜的反应为
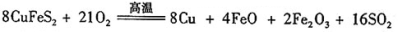
若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是 (填元素符号)。当生成0.8 mol铜时,此反应转移的电子数目是___________________。
I、 (1)4 1 4 4 2H2O (2分) (2)FeS2(1分) (3)硫酸亚铁和硫酸(1分)
II、2I-+ClO-+H2O = I2 + Cl-+2OH- (2分)
I2 + 5ClO-+2OH- = 2IO3-+ 5Cl-+H2O (2分) ClO->IO3->I2(1分)
III、Cu、O(2分); 10NA(2分)
【解析】
试题分析:I、(1)根据元素守恒,可知反应②的另一种生成物为H2O,根据氧化还原反应中,化合价升高的总价数等于化合价降低的总价数,配平可得离子方程式为:4Fe2++O2+4H+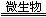 4Fe3++2H2O。
4Fe3++2H2O。
(2)还原剂是元素化合价反应后升高,反应③中硫元素化合价从-1价变化为0价,所以反应中的还原剂是FeS2。
(3)依据①②③④的离子方程式,分析判断最终的生成物为硫酸亚铁和硫酸。
II、在KI淀粉溶液中滴入少量NaClO溶液,溶液立即变蓝,说明生成碘,NaClO氧化KI生成碘,反应的离子方程式为2I-+ClO-+H2O = I2 + Cl-+2OH-,所以氧化性ClO->I2;继续滴加足量的NaClO溶液,蓝色逐渐消失,说明碘与NaClO发生氧化还原反应,反应的离子方程式为I2 + 5ClO-+2OH- = 2IO3-+ 5Cl-+H2O,氧化剂是ClO-,还原剂是I2,氧化产物是 IO3-,所以氧化性ClO->IO3->I2。
III、反应8CuFeS2+21O2 8Cu+4FeO+2Fe203+16SO2中铜元素、氧元素在得电子化合价降低,被还原;设转移电子数为x,
8Cu+4FeO+2Fe203+16SO2中铜元素、氧元素在得电子化合价降低,被还原;设转移电子数为x,
8CuFeS2+21O2 8Cu+4FeO+2Fe203+16SO2 转移电子
8Cu+4FeO+2Fe203+16SO2 转移电子
8mol 100NA
0.8mol x
解得x=10NA。
考点:本题考查氧化还原反应的电荷守恒、原子守恒的应用、离子方程式的书写、化学计算。


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源:2015届山东省文登市高三上学期11月月考化学试卷(A卷)(解析版) 题型:选择题
下列物质与足量铁反应,转移电子数最少的是
A.1mol氯气 B.1mol S
C.含1molHNO3的稀硝酸 D.含1molCuSO4的硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源:2015届山东省德州市高三10月月考化学试卷(解析版) 题型:选择题
用36.5%的浓盐酸(密度1.2 g·cm-3)配1 mol·L-1的稀盐酸 100 mL,配制过程需用到哪些仪器,且先后顺序正确的是
①100 mL量筒 ②10 mL量筒 ③50 mL 烧杯 ④托盘天平 ⑤100 mL容量瓶
⑥胶头滴管 ⑦玻璃棒
A.①③⑤⑥⑦ B.②③⑦⑤⑥ C.③⑤⑦⑥① D.④③⑦⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次模拟考试试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数,下列叙述正确的是
A.1 mol Cl2在反应中得到电子数不一定为2NA
B.1 mol O2在反应中得到电子数一定为4 NA
C.1 mo1 Na2O2与足量H2O反应,转移了2 NA 个电子
D.在2KClO3+4HC1(浓)==2KCl+2C1O2↑+C12↑+2H2O中,氯气既是氧化产物又是还原产物
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次模拟考试试卷(解析版) 题型:选择题
下列关于金属钠的叙述错误的是
A.金属钠可以保存在煤油中
B.金属钠着火时,可用泡沫灭火器来灭火
C.钠与熔融的四氯化钛反应可制取钛
D.实验时用剩的钠块应该放回原试剂瓶
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三11月阶段模块考试化学试卷(解析版) 题型:选择题
X、Y、Z是位于不同周期的三种短周期元素,且原子序数逐渐增大,X、Z属于同一主族,三种元素可以形成原子个数比为1:1:1的化合物W。下列推测正确的是
A.元素Z的氧化物一定属于碱性氧化物
B.原子半径关系是:X<Y<Z
C.三种元素中,Y的金属性最强
D.Y、Z都能形成含氧酸,且前者的酸性比后者酸性强
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三11月阶段模块考试化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.用丁达尔现象实验可以区分食盐水和淀粉溶液
B.氨气的水溶液能导电,所以氨气是电解质
C.NO2、SO2溶于水都发生氧化还原反应
D.Fe分别与氯气和稀盐酸反应可得到同一种氯化物
查看答案和解析>>
科目:高中化学 来源:2015届山东省乐陵市高三10月初检测化学试卷(解析版) 题型:选择题
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeC13溶液 ③Zn与H2SO4溶液 ④Fe与HC1溶液,由于浓度不同而能发生不同氧化还原反应的是( )
A.①③ B.③④ C.①② D.①③④
查看答案和解析>>
科目:高中化学 来源:2015届山东淄博市高三上学期第二次诊断性检测理综化学试卷(解析版) 题型:选择题
下列各组离子在指定溶液中能大量共存的是
A.使酚酞变红色的溶液:Fe3+、Mg2+、SO42-、NO3-
B.KNO3的酸性溶液:Fe2+、Ca2+、Al3+、Cl-
C.常温下,由水电离出的c(H+)=1.0×10-10 mol·L-1的溶液:NH4+、Na+、SiO32-、CO32-
D.透明的溶液:Cu2+、Fe3+、NO3-、MnO4-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com