
分析 (1)反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
根据盖斯定律,得反应Ⅲ=反应Ⅱ×2-反应Ⅰ;
故答案为:2△H2-△H1;
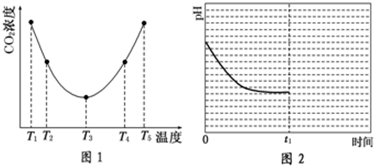
(2)①温度升高,c(CO2)增大,平衡逆向移动,说明反应Ⅲ是放热反应(△H3<0);②T1-T2区间,化学反应未达到平衡状态,温度越高,化学反应速率越快,所以CO2被捕获的量随着温度的升高而提高.T3-T4区间,化学反应已达到平衡状态,由于正反应为放热反应,温度升高平衡向逆反应方向移动,所以不利于CO2的捕获
③反应Ⅲ在温度为T1时建立平衡后(由图2可知:溶液pH不随时间变化而变化),迅速上升到T2并维持温度不变,平衡逆向移动,溶液pH增大,在T2时又建立新的平衡;
(3)根据平衡移动原理分析.
解答 解:(1)反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
根据盖斯定律,得反应Ⅲ=反应Ⅱ×2-反应Ⅰ,所以△H3与△H1、△H2之间的关系是:△H3=2△H2-△H1;故答案为:2△H2-△H1;
(2)①由图1可知:温度为T3时反应达平衡,此后温度升高,c(CO2)增大,平衡逆向移动,说明反应Ⅲ是放热反应△H3<0;
②在T3前反应未建立平衡,无论在什么温度下(NH4)2CO3 (aq)总是捕获CO2,故c(CO2)减小;
③反应Ⅲ在温度为T1时建立平衡后(由图2可知:溶液pH不随时间变化而变化),迅速上升到T2并维持温度不变,平衡逆向移动,溶液pH增大,在T2时又建立新的平衡,图象应为,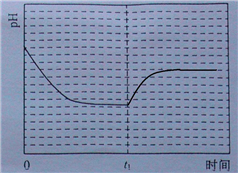 ;
;
故答案为:①<;
②T1-T2区间,化学反应未达到平衡,温度越高,化学反应的速率越快,所以CO2被捕获的量随温度升高而提高.T4-T5区间,化学反应已达到平衡,由于正反应是放热反应,温度升高平衡向逆反应方向移动,所以不利于CO2的捕获;
③
(3)根据平衡移动原理,降低温度或增大c(CO2),故答案为:降低温度;增大CO2浓度.
点评 本题考查热化学方程式书写,化学反应速率、化学平衡移动和化学方程式书写等,题目综合性较强.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
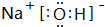 .
.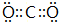 .属非极性分子(填分子极性).EC2其固体属原子晶体.
.属非极性分子(填分子极性).EC2其固体属原子晶体. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二者对应的氧化物均为碱性氧化物 | |
| B. | 二者的单质都能与强碱溶液反应生成H2 | |
| C. | 二者的氢氧化物均可以通过化合反应直接制备 | |
| D. | 二者的氯化物均可以通化合反应制备 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 0~2分钟、2~3分钟内用A浓度表示的平均反应速率:v(0~2)>v(2~3)>0 | |
| B. | 容器中发生的反应可表示为:3A(g)+B(g)?2C(g) | |
| C. | 若X表示温度,则生成C的反应是放热反应 | |
| D. | 若其他条件不变,仅减小起始时B的浓度,开始反应后C物质的浓度一定减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com