
| A. | 通入过量的NH3(g):Ag+、NH4+、NO3-、OH- | |
| B. | 加入过量 HNO3(aq):NH4+、Ag+、H+、NO3- | |
| C. | 通入过量 HCl(g):NH4+、H+、Cl-、NO3- | |
| D. | 加入过量NaOH(aq):NH4+、Na+、NO3-、OH- |
分析 葡萄糖发生银镜反应为:CH2OH(CHOH)4CHO+2Ag(NH3)2OH $\stackrel{△}{→}$CH2OH(CHOH)4COONH4+2Ag↓+H2O+3NH3,过滤后溶液含Ag(NH3)2+、NH4+,结合离子之间的反应来解答.
解答 解:葡萄糖发生银镜反应为:CH2OH(CHOH)4CHO+2Ag(NH3)2OH $\stackrel{△}{→}$CH2OH(CHOH)4COONH4+2Ag↓+H2O+3NH3,过滤后溶液含Ag(NH3)2+、NH4+,
A.通入过量的NH3,不能存在OH-,故A错误;
B.加入过量 HNO3(aq),与Ag(NH3)2OH反应,溶液中含NH4+、Ag+、H+、NO3-,故B正确;
C.通入过量 HCl(g),与Ag(NH3)2OH反应,溶液中含NH4+、H+、Cl-,故C错误;
D.加入过量NaOH(aq),不能大量存在NH4+,故D错误;
故选B.
点评 本题考查离子共存,为高考常见题型和高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意银氨溶液的成分,题目难度不大.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:选择题
| A. | K +、.MnO 4 -、Cl -、SO 4 2- | B. | Na +、CO 3 2-、Cl -、SO 4 2- | ||
| C. | NO 3 -、Na +、HCO 3 -、Ba 2+ | D. | Na +、NO 3 -、NH 4 +、SO 4 2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 元素的非金属性次序为c>b>a | |
| B. | a-的还原性弱于c-的还原性 | |
| C. | d和其他3种元素均能形成离子化合物 | |
| D. | 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 95℃纯水的 pH<7,说明加热可导致水呈酸性 | |
| B. | pH=3的醋酸溶液,稀释至 10 倍后 pH=4 | |
| C. | pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH>7 | |
| D. | pH 均为3的醋酸和盐酸分别与足量Zn反应,醋酸产生的H2多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酶属于碳水化合物,是生物体中重要的催化剂 | |
| B. | 纤维素为天然高分子化合物,遇碘水会变蓝色 | |
| C. | 某些卤代烃能破坏臭氧层,使卤代烃的使用受到限制 | |
| D. | 某有机物的1H核磁共振谱图中特征峰的数目就是氢原子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | 先加硝酸,再滴加BaCl2溶液 | 产生白色沉淀 | 原溶液中一定有SO42- |
| B | 先加入H2O2溶液,再加KSCN溶液 | 溶液呈血红色 | 原溶液中一定有Fe2+ |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中一定有Na+、无K+ |
| D | 滴加NaOH溶液,加热,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 原溶液中一定有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸的结构简式 C2H4O2 | B. | 氯化钠的电子式: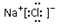 | ||
| C. | 硫原子的原子结构示意图: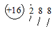 | D. | 水的电离方程式 2H2O═H3O++OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com