
����Ŀ�������ӵĹ�ҵ��ˮ�Ĵ���������ͼ��ʾ��

��1��������ͼ�豸���н��е��Dz���________(��д��������)��ʵ��������һ������������_______(����������)���С�
�����豸�������豸��������A��______________(�ѧʽ����ͬ)�����豸�������豸��������B��___________��
�����豸���з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��
�����豸���У�����B��ˮ��Һ��CaO��Ӧ������NaOH��H2O��______��ͨ�� _________________(���������)����������ʹ��������롣
��ͼ�У���ѭ��ʹ�õ�������_______��_____________C6H6��CaO��
��2��Ϊ�˷�ֹˮԴ��Ⱦ���ü����������Եķ�������ij�����ŷŵ���ˮ�����ޱ��ӣ��˷�����____________��
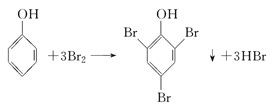
�ӷ�ˮ�л��ձ��ӵķ����Ǣ����л��ܼ���ȡ��Һ�еı��ӣ��ڼ���ij��ҩƷ��ˮ��Һʹ�������л��ܼ����룻�ۼ���ij�������������ӡ���д�������������ķ�Ӧ����ʽ��_________________________��
��3��Ϊ�ⶨ��ˮ�б��ӵĺ�����ȡ�˷�ˮ100 mL�������м���Ũ��ˮ�����ٲ�������Ϊֹ���õ�����0.331 g����˷�ˮ�б��ӵĺ���____________(mg��L��1)��
���𰸡� ��ȡ����Һ ��Һ©�� C6H5ONa NaHCO3 C6H5ONa��CO2��H2O�D��C6H5OH��NaHCO3 CaCO3 ���� NaOH��Һ CO2 ����ˮ�еμ�FeCl3��Һ������Һ����ɫ���������ˮ���б��� 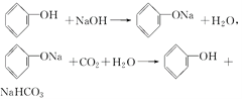 940 mg��L��1
940 mg��L��1
������������һ������ʵ���⣬��Ҫ���鱽�ӵ���������ѧ���ʺ���ȡ����Һ�IJ��������ȣ�Ҫ��ȷ��������ͼ���Լ������ã��ٽ�ϱ��ӵ����ʺͻ���ʵ������Ϳ�һһ���
(1)�豸�����ˮ�ͱ���Ϸ����ˮ����Ȼ����ȡ������ʵ�����п����÷�Һ©�����У��豸�����Ӻͱ��Ļ��Һ�м���NaOH��Һ��Ŀ���Ƿ����������A�����DZ�������Һ�����豸����ͨ��CO2��������ӣ���ʣ������B��NaHCO3��Һ�����豸������NaHCO3��Һ�м���CaO������NaOH��H2O��CaCO3�����ù��˲��������CaCO3�����豸���м���CaCO3�ɵ�CO2��CaO��(3)��ÿ����ˮ�����ӵ�����Ϊx��
94 ������ ���������� 331
x �������� ���� 0.331g��10
x �� 0.94 g��
���Դ˷�ˮ�б��ӵĺ���Ϊ940mg��L��1��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ������г����۵�ij��ʳ�þ����ΰ�װ����������˵����

���������⻯����ϡ�����ữ�����·������·�Ӧ��KIO3��5KI�� 5H2SO4��3K2SO4�� 3I2��3H2O
������λͬѧ�ֱ��ò�ͬ�ķ������������100mL 3.6molL��1��ϡ���ᡣ
��1��������18molL��1��Ũ����������Һ����Ҫ����Ͳ��ȡŨ��������Ϊ_______mL��
��2����ѧ������ȡŨ���ᣬ���ձ���ϡ�ͣ���ȴ�����º�ת�Ƶ�100mL����ƿ�У�ϴ�ӣ�Ȼ���ݣ�����ƿ�����������µߵ�ҡ�ȡ����ƹ����ж���õ�������������Ҫ������______________________��
��3����ʵ���н������в���ʹ������Һ�����ʵ���Ũ��ƫ�ߵ���_____________��
�ٶ���ʱ�۲�Һ�温�Ӣ�δ����ȴ���Ƚ���Һע������ƿ��
��ҡ�Ⱥ���Һ����ڿ̶����ټ�ˮ������ƿ��ԭ����������ˮ
��4����ѧ������100mL��Ͳ��ȡŨ���ᣬ��������С�ĵؼ�������ˮ��������ȣ�����ȴ�����º��ټ�ˮ��100mL�̶��ߣ�������ȣ�����Ϊ�˷��Ƿ���ȷ��������ȷ��ָ�����д���֮��__________________��
������֪������Ӧ���ɵ�I2�ɷ������·�Ӧ��I2��2S2O32����2I����S4O62����ijѧ���ⶨʳ�þ����εĵ⺬�����䲽��Ϊ��a.ȷ��ȡw gʳ�Σ�����������ˮʹ����ȫ�ܽ⣻b����ϡ�����ữ������Һ����������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��c���Ե�����ҺΪָʾ������μ������ʵ���Ũ��Ϊ1.0��10-3mol/L ��Na2S2O3��Һ20.0 mL��ǡ�÷�Ӧ��ȫ��
��1��b�з�Ӧ��������I2�����ʵ�����________ mol��
��2����������ʵ��Ͱ�װ��˵�������⾫���εĵ⺬����_______________ mg/kg��(�Ժ�w�Ĵ���ʽ��ʾ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���Ʊ��ߴ����ж��ַ��������е�һ�ֹ����������£�

��֪����������Ӧ�IJ����У���SiCl4�⣬����SiHCl3��SiH2Cl2��SiH3Cl��FeCl3�ȡ�����˵����ȷ����
A. �绡¯�з����ķ�ӦΪC��SiO2![]() CO2����Si
CO2����Si
B. SiCl4���뻹ԭ¯֮ǰ��Ҫ���������ᴿ
C. ÿ����l mol�ߴ��裬��Ҫ44. 8L Cl2����״����
D. �ù���Si�IJ��ʸߣ�������ɫ��ѧҪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�л���A��NaOH�Ĵ���Һ��ϼ��ȵò���C����ҺD��C����ϩ����ڴ��������¿ɷ�Ӧ����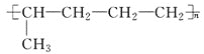 �ĸ߾��������ҺD���ȼ��������ữ�����AgNO3��Һ�а�ɫ�������ɣ���A�Ľṹ��ʽ����Ϊ(����)
�ĸ߾��������ҺD���ȼ��������ữ�����AgNO3��Һ�а�ɫ�������ɣ���A�Ľṹ��ʽ����Ϊ(����)
A. 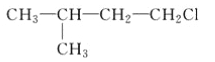 B.
B. 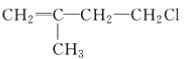 C. CH3CH2CH2ClD.
C. CH3CH2CH2ClD. 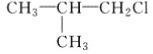
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ƿ��ֽ��Ǵ�������һ�ֳ�֮Ϊ�ʻ���(COS)�ķ��ӣ���ṹ��CO2���ƣ��ʻ�����һ��������������ص����ʣ������Ʋⲻ��ȷ����( )
A. COS�Ǻ��м��Լ��Ĺ��ۻ�����B. COS�ķе��CO2��
C. COS ����ʽΪ![]() D. COS������ԭ������8�����ȶ��ṹ
D. COS������ԭ������8�����ȶ��ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.Na2O��Na2O2���Ԫ����ͬ����CO2��Ӧ����Ҳ��ͬ
B.��CO2ͨ��BaCl2��Һ������BaCO3����
C.��CO2ͨ����������Һ�����ɴ�����
D.0.12gʯī�к���6.02��1022��̼ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�� W��X��Y��Zԭ��������������W��Y��X��Zλ��ͬһ���壬W��X���γɹ��ۻ����� WX2��Yԭ���ڲ������������������������2.5����������������ȷ���ǣ� ��
A. WX��WX2��ZX2�Ļ�ѧ��������ȫ��ͬ
B. WZ2����������ԭ������㶼����8���ӽṹ
C. ����X�ij����⻯�H2X�����Ӽ�����������H2X��H2Z �ȶ�
D. ԭ�Ӱ뾶��С˳��ΪX<W<Z<Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в������Լ���ѡ������������ �� ��
A. ��˿�ܴ��沬˿������ɫ��Ӧʵ��B. ����ƿ������ˮϴ�Ӻ����ɲ���ʹ��
C. �÷�Һ©������ˮ��CCl4�����D. ��Ʒ����Һ����SO2��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ����4��̼ԭ�ӽ�ϳɵ�4����(��ԭ��û�л���)��

(1)д���л���(a)��ϰ�������������ƣ�________��
(2)�����л����У�������̼ԭ��һ����ͬһƽ�����______________��______________(��ṹ��ʽ)��
(3)�����л����в�������ˮ������Ӧʹ����ɫ����______(����ĸ����)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com