

分析 (1)电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液,由图可知,右侧生成氢气,则B中氢离子放电,可知B为阴极,在B中制备LiOH,Li+由A经过阳离子交换膜向B移动;A中为LiCl溶液,氯离子放电生成氯气;
(2)Co(OH)3溶解还原反应为Co(OH)3、H+、SO32-的氧化还原反应;由制备流程可知,加硫酸溶解后为铁离子,再与亚硫酸钠发生氧化还原反应生成亚铁离子,在浸液中通入氧气时亚铁离子被氧化为铁离子;煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),n(CO2)=$\frac{1.344L}{22.4L/mol}$=0.06mol,由化学式可知n(Co)=0.06mol×$\frac{1}{2}$=0.03mol,则氧化物中n(O)=$\frac{2.41g-0.03mol×59g/mol}{16g/mol}$=0.04mol,以此来解答.
解答 解:(1)电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液,由图可知,右侧生成氢气,则B中氢离子放电,可知B为阴极,在B中制备LiOH,B极区电解液为LiOH溶液;Li+由A经过阳离子交换膜向B移动;A中为LiCl溶液,氯离子放电生成氯气,则阳极反应式为2Cl--2e-=Cl2↑,
故答案为:LiOH;2Cl--2e-=Cl2↑;B;
(2)Co(OH)3溶解还原反应为Co(OH)3、H+、SO32-的氧化还原反应,其离子反应为2Co(OH)3+4H++SO32-=2Co2++SO42-+5H2O;由制备流程可知,加硫酸溶解后为铁离子,再与亚硫酸钠发生氧化还原反应生成亚铁离子,在浸液中通入氧气时亚铁离子被氧化为铁离子,可知铁渣中铁元素的化合价为+3价;煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),n(CO2)=$\frac{1.344L}{22.4L/mol}$=0.06mol,由化学式可知n(Co)=0.06mol×$\frac{1}{2}$=0.03mol,则氧化物中n(O)=$\frac{2.41g-0.03mol×59g/mol}{16g/mol}$=0.04mol,则n(Co):n(O)=0.03mol:0.04mol=3:4,所以钴氧化物的化学式为Co3O4,
故答案为:2Co(OH)3+4H++SO32-=2Co2++SO42-+5H2O;Co3O4.
点评 本题为2015年山东高考题29题,侧重电化学、物质制备及混合物分离提纯的考查,把握原电池原理及制备流程中的反应为解答的关键,(2)中化学式的计算为解答的难点,题目难度不大.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和苯都能发生取代反应 | |
| B. | 乙醇和乙酸都能与氢氧化钠发生中和反应 | |
| C. | 乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应 | |
| D. | 淀粉、油脂、蛋白质都属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 100:1 | C. | 1:100 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 4:3:2 | B. | 1:2:1 | C. | 2:1:1 | D. | 1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 它属于( )
它属于( )| A. | ①③④ | B. | ①③⑤ | C. | ②③⑤⑥ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 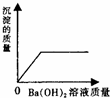 | B. | 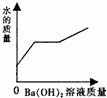 | C. | 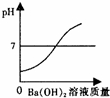 | D. | 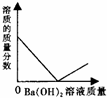 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
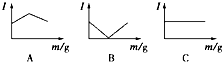 在一定温度下向不同电解质溶液中加入新物质时溶液的导电性能发生变化,如下图所示是其电流(Ⅰ)随新物质加入量(m)的变化曲线.
在一定温度下向不同电解质溶液中加入新物质时溶液的导电性能发生变化,如下图所示是其电流(Ⅰ)随新物质加入量(m)的变化曲线.| A | B | C | |
| A | ① | ② | ③ |
| B | ④ | ②③ | ① |
| C | ③ | ①② | ④ |
| D | ② | ①③ | ④ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COOˉ)>c(CO32-) | |
| B. | 随着CO2的通入,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$不断增大 | |
| C. | 在溶液中pH不断降低的过程中,有含NH2COOˉ的中间产物生成 | |
| D. | 不同pH的溶液中有:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COOˉ)+c(OHˉ) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com