
在中学化学实验中使用的玻璃、陶瓷等仪器,在实验操作中不能承受温度的急剧变化,否则会引起安全事故。下列实验操作过程不是基于上述原因的是( )
A.钠与水反应时,只能取黄豆粒大小的钠投入盛水的烧杯中反应
B.在用二氧化锰和浓盐酸制氯气时,在加入二氧化锰后应首先加入浓盐酸,然后再点燃酒精灯
C.在用固体氯化铵和氢氧化钙制取氨气结束后,将大试管从铁架台上取下置于石棉网上冷却后再洗涤
D.用排水法收集气体后,先移出导气管,后熄灭酒精灯
科目:高中化学 来源: 题型:
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如图所示。

(1)X的单质与A反应的化学方程式是 。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是 。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示) 。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关环境方面的说法不正确的是( )
A.CO能使人中毒的原理是CO能将人体血液中的Fe2+氧化
B.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,提高空气质量
C.推广可利用太阳能、风能等新能源,发展低碳经济,同时能大大减少对环境的污染
D.PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重
查看答案和解析>>
科目:高中化学 来源: 题型:
有如下几种制备气体的方案:
①用稀硝酸与锌粉反应制氢气;②用水与过氧化钠固体反应制氧气;③常温下用铁片和浓硫酸制备二氧化硫;④氧化钙与浓氨水反应制氨气。不宜采用的方案有
( )
A.①③ B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
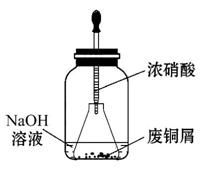
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式_________________________________。
(2)上图装置中NaOH溶液的作用是____________________________________。
(3)步骤二中,水浴加热所需仪器有____________、____________(加热、夹持仪器、石棉网除外),水浴加热的优点是_________________________________。
(4)若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验方案或操作正确的是( )
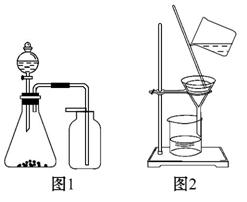
A.选择合适的试剂,用图1装置可分别制取和收集少量CO2、NO
B.除去石英(主要成分SiO2)中少量碳酸钙:用稀盐酸溶解后过滤
C.洗涤沉淀时(见图2),向漏斗中加适量水,搅拌并滤干
D.用广范pH试纸测得0.1 mol·L-1NH4Cl溶液pH=5.2
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列各装置图的叙述不正确的是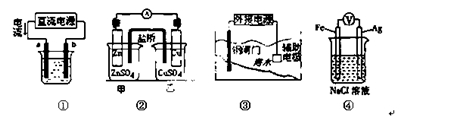
A.用图①装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液
B.图②装置的盐桥中KCl的Cl—移向甲烧杯
C.图③装置中钢闸门应与外接电源的负极相连获得保护
D.装置④中Ag电极发生反应:2H 2O + 2e- = H2↑+ 2OH-
2O + 2e- = H2↑+ 2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH 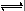 CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)下列方法中,可以使0.10 mol·L-1 CH3COOH 的电离程度增大的是 。
的电离程度增大的是 。
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2) pH值相同的 ①HCl(aq)、②H2SO4(aq)、 ③CH3COOH(aq)各100 mL
分别用0.1 mol/L的NaOH(aq)中和,消耗NaOH(aq)的体积分别为V1、V2、V3,它们由大到小的顺序是 。
(3) 物质的量浓度相同的①HCl(aq)、②H2SO4(aq)、 ③CH3COOH(aq)各
100mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、
V2、V3,它们由大到小的顺序是 。
bcf (2)V1=V2<V3 (3)V1= V3<V2
V3<V2
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组只领取下列仪器(或用品):铁架台(带铁夹、铁圈)、三角架、石棉网、烧杯、漏斗、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、火柴、滤纸。只应用上述仪器用品,不能进行的实验操作是( )
A.蒸发 B.萃取 C.过滤 D.蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com