
 2SO3(g),该反应在体积不变的密闭容器中进行,则下列 (填序号)可作为反应达到平衡的判断依据。
2SO3(g),该反应在体积不变的密闭容器中进行,则下列 (填序号)可作为反应达到平衡的判断依据。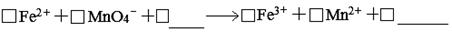
 2Fe2O3 + 8SO2 (2) B C D(少对一个扣1分,有错计0分) (3) 冷凝管 (4)B D(对一个计1分,有错计0分)
2Fe2O3 + 8SO2 (2) B C D(少对一个扣1分,有错计0分) (3) 冷凝管 (4)B D(对一个计1分,有错计0分)  2Fe2O3 + 8SO2 ;
2Fe2O3 + 8SO2 ;

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源:不详 题型:单选题
| A.研究一种新材料的性质和用途 | B.研究一种新微粒的组成和结构 |
| C.研究一种新药品的合成 | D.研究一种新物质的运动规律 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.自来水可以用氯气杀菌消毒,因为氯气具有强氧化性、漂白性 | |
| B.加热能杀死甲型H1N1流感病毒是因为病毒的蛋白质受热变性 | |
C.工业上用热还原法冶炼太阳能电池板中的硅 | D.随意丢弃废旧电池,会导致水体和土壤重金属污染 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.所得物质一定为悬浊液 | B.所得物质一定为乳浊液 |
| C.有丁达尔效应 | D.能透过滤纸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
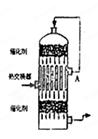
| A.SO2 | B.SO3、O2 | C.SO2、SO3 | D.SO2、O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯碱工业中的阳离子交换膜阻止阳离子通过 |
| B.生产普通玻璃的主要原料有石灰石、石英和纯碱 |
| C.工业上将粗铜进行精炼,应将粗铜连接在电源的正极 |
| D.工业上,用焦炭在电炉中还原二氧化硅得到含少量杂质的粗硅 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用汽油、煤油除去油污时发生的主要是物理变化 |
| B.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 |
C.在含硫的燃料中加入适量生石灰,以减少二氧 化硫的排放量 化硫的排放量 |
| D.棉花、蚕丝和人造丝的主要成分都是纤维素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com