
A.一定是金属元素 B.一定是ⅡA族元素
C.一定是过渡元素 D.可能是金属元素,也可能不是金属元素
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解

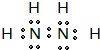
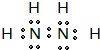
| 电离能I(eV) | A | B | C | D | E | F |
| I1 | 11.3 | 14.5 | 13.6 | 5.2 | 7.6 | 6.0 |
| I2 | 24.4 | 29.6 | 35.1 | 49.3 | 15.0 | 18.8 |
| I3 | 47.9 | 47.4 | 54.9 | 71.6 | 80.1 | 28.4 |
| I4 | 64.5 | 77.5 | 77.4 | 98.9 | 109.2 | 112.0 |
| I5 | 392.1 | 97.9 | 113.9 | 138.3 | 141.3 | 153.7 |
查看答案和解析>>
科目:高中化学 来源:山东临沂市2006-2007高三上学期期中统一考试、化学 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
1.《有机化学基础》芬必得是一种高效的消炎药,其主要成分为布洛芬,它有多种合成路线,如图就是一种合成方法。
已知卤代烃有如下反应:R—Cl+NaCN![]() R—C≡N+NaCl。
R—C≡N+NaCl。

回答下列问题:
(1)写出D的结构简式:____________________。
(2)写出反应类型:A→B____________,B→C____________。
(3)C和苯酚的关系是____________。
a.互为同分异构体 b.互为同系物
c.均为芳香族化合物 d.均属于芳香烃
(4)写出C发生消去反应的化学方程式(注明反应条件):__________________________。
(5)与A具有相同分子式,且苯环上只有一个取代基的有机物共有四种,除A的结构外,写出其余三种结构简式中的任意两种:
_____________________________、____________________________。
2.《物质结构与性质》纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。
A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 932 | 1 821 | 15 390 | 21 771 |
B | 738 | 1 451 | 7 733 | 10 540 |

(1)某同学根据上述信息,推断B的核外电子排布如上图所示,该同学所画的电子排布图违背了____________。
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为____________。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
(4)已知金刚石中的C—C的键长为154.45 pm,C60中C—C键长为145—140 pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由_________________________。
(5)科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为____________。
(6)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是__________。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为____________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:填空题
在一百多种化学元素中,非金属占了23种。80%的非金属元素在社会中占重要位置。如C、N、O、Si、Cl等。
(1)氯元素原子最外电子层上有 种能量不同的电子,该元素的简单阴离子核外电子排布式是 。
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件,因为它属于 晶体,请写出该化合物的化学式 。
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有 。(选填编号)
a.Cl原子最外层电子数比氧多
b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为−2价
d.沸点:H2O>HCl
与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:NaClO2 +HCl ClO2↑+___________________(没有配平)
ClO2↑+___________________(没有配平)
(4)上述方程式中,缺项物质是___________,配平方程式,并在下面补全反应物系数。____NaClO2 +____HCl
(5)该反应中氧化剂和还原剂的物质的量之比是 。生成0.2 mol ClO2转移电子的物质的量为 _______ mol。
(6)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某污水中含CN-a mg/L,现用ClO2将CN-氧化,只生成两种无毒气体。处理100m3这种污水,至少需要ClO2 _______ mol 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com