
�״���һ�ֿ�����ȼ�ϡ����ݻ�Ϊ2L���ܱ������н��з�Ӧ��CO(g)+2H2(g) CH3OH(g) �������������䣬��300���500��ʱ�����ʵ���n(CH3OH)-��Ӧʱ��t�ı仯������ͼ��ʾ��
CH3OH(g) �������������䣬��300���500��ʱ�����ʵ���n(CH3OH)-��Ӧʱ��t�ı仯������ͼ��ʾ��

��1���÷�Ӧ�ġ�H 0 ����>��<��=��
��2��300��ʱ��0-t1 min�� CH3OH��ƽ����������Ϊ
��3����Ҫ��״��IJ��ʣ��ɲ�ȡ�Ĵ�ʩ��_________ ��������ĸ��
A����С������� B�������¶�
C�������¶� D��ʹ�ú��ʵĴ���
E���״��ӻ����ϵ�з������
��4��300��ʱ��CO��H2����ʼ���ʵ����ֱ�Ϊ2mol��3mol����ͼ��n1����Ϊ0.5mol���Լ���300���£��÷�Ӧ��ƽ�ⳣ����д��������̣�������λ��Ч���֣�
��5����ҵ��Ҳ������CO2��H2��Ӧ�Ƶü״�����2��105Pa��300��������£�����440g CO2��H2ǡ����ȫ��Ӧ���ɼ״���ˮ���ų�495kJ����������д���÷�Ӧ���Ȼ�ѧ����ʽ ��
��֪ʶ�㡿��ѧƽ����ƶ�����ѧƽ��ļ��㡢�Ȼ�ѧ����ʽ����д G2 F2
���𰸽�����
(1)�� (2)n1/2t1 mol·L-1·min-1 (3��ABE
(4) CO(g)+2H2(g) CH3OH
CH3OH
��ʼ���ʵ���Ũ�ȣ�mol·L-1) 1.0 1.5 0
ת�����ʵ���Ũ�ȣ�mol·L-1) 0.25 0.5 0.25
ƽ�����ʵ���Ũ�ȣ�mol·L-1) 0.75 1.0 0.25
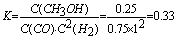
(5)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ��H=-49.5KJ/mol
������(1)����ͼ��500���300��ƽ��ʱ�״������ʵ���С��˵�������¶�ƽ���������ƶ�������Ӧ�Ƿ��ȷ�Ӧ���÷�Ӧ�ġ�H��0��
��2��300��ʱ��0-t1 min�� CH3OH��ƽ����������Ϊ��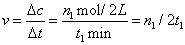 mol·L-1·min-1
mol·L-1·min-1
��3����Ҫ��״��IJ��ʣ�Ҳ����ʹƽ�������ƶ����ɲ�ȡ�Ĵ�ʩ�У���ѹ�����¡���С�״���Ũ�ȣ��������¶�ƽ�������ƶ����״��IJ��ʽ��ͣ�ʹ�ô���ƽ�ⲻ�ƶ�������ѡABE��
��4����������ʽ����ƽ��ʱ��Ӧ�P�������Ũ�ȣ�����ƽ�ⳣ������ʽ���ɡ�
��5������440g CO2��H2ǡ����ȫ��Ӧ���ɼ״���ˮ���ų�495kJ������������44g CO2��H2ǡ����ȫ��Ӧ���ɼ״���ˮ���ų�49.5kJ������,�÷�Ӧ���Ȼ�ѧ����ʽΪ��CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ��H=-49.5KJ/mol
��˼·�㲦�����⿼���˻�ѧƽ����ƶ�����ѧƽ��ļ��㡢�Ȼ�ѧ����ʽ����д���ѶȲ���


 �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
.��ij���ᴦ������ʯʱ����õ�һ�ֳ������ó�����X��Y��Z��W���ֶ�����Ԫ����ɣ����Ļ�ѧʽΪXYZW6������X��Y��Zλ��ͬһ������������������������Y2+��W-������ͬ���Ӳ�ṹ������˵����ȷ����
A. ���Ӱ뾶��Y2+>W- B. ԭ�Ӱ뾶��X>Y>Z>W
C. ���ʷе㣺X>Y>Z>W D.����Ԫ�صļ����Ӿ����ƻ�ˮ�ĵ���ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)д�����л���������ƻ�ṹ��ʽ��

(2)������ֳƻƼ���ҹ��ض�����ҩ������������е�һ���������ҹ���ѧ���о�������ṹ���£�
��������к��������ŵ�������________������________��(������ӡ�)��
�����и����ʣ�
 ������ػ�Ϊͬ���칹�����________(����ĸ����ͬ)����Ϊͬϵ�����________��
������ػ�Ϊͬ���칹�����________(����ĸ����ͬ)����Ϊͬϵ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��ڵ������Һ�����ӹ�ϵ��˵����ȷ����(����)
A��0.1 mol��L��1NaHCO3��Һ������Ũ�ȹ�ϵ��c(Na��)��2c(CO )��c(HCO
)��c(HCO )��c(H2CO3)
)��c(H2CO3)
B��0.1 mol��L��1 NH4Cl��0.1 mol��L��1 NH3��H2O�������Ϻ�����Ũ�ȹ�ϵ��c(Cl��)��c(NH )��c(H��)��c(OH��)
)��c(H��)��c(OH��)
C�������£����������Һ�еμ���������ʹ��Һ��pH��7��������Һ�У�c(Na��)��c(CH3COO��)
D�������£���pH��1����Һ�У�Fe2����NO ��ClO����Na���ܴ�������
��ClO����Na���ܴ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)�����ͬ��Ũ�Ⱦ�Ϊ0.2 mol��L��1�������CH3COOH��Һ���ֱ��ˮϡ��10������Һ��pH�ֱ���m��n����m��n�Ĺ�ϵΪ________��
(2)�����ͬ��Ũ�Ⱦ�Ϊ0.2 mol��L��1�������CH3COOH��Һ���ֱ��ˮϡ��m����n������Һ��pH�����3����m��n�Ĺ�ϵΪ________��
(3)�����ͬ��pH������1�������CH3COOH��Һ���ֱ��ˮϡ��m����n������Һ��pH�����3����m��n�Ĺ�ϵΪ________��
(4)�����ͬ��pH������13�İ�ˮ��NaOH��Һ���ֱ��ˮϡ��m����n������Һ��pH�����9����m��n�Ĺ�ϵΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
)����ȼ�ϵ����Ŀǰ��Ϊ�����ȼ�ϵ�أ��������ɺͷ�Ӧԭ�����¡�

��1���ڸ���������Ҫ�����ķ�ӦΪ_______________________________
��2����λ��Ӧ����CO(g)+H2O (g)  CO2 (g)+H2(g) ����һ���¶��£���1L�����з���������Ӧ�������ʵ����ʵ���Ũ�ȱ仯���±���
CO2 (g)+H2(g) ����һ���¶��£���1L�����з���������Ӧ�������ʵ����ʵ���Ũ�ȱ仯���±���
| t/min | COmol/L) | H2O(mol/L) | CO2(mol/L) | H2(mol/L) |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.1 |
| 3 | n1 | n2 | n3 | 0.1 |
| 4 | 0.09 | 0.19 | 0.11 | 0.11 |
�ٴ��¶��£��÷�Ӧ��ƽ�ⳣ��Ϊ________
�ڷ�Ӧ��3��4 min֮�䣬���������ʵ��������ԭ������� ������ţ�
A������ˮ���� B�������¶� C��ʹ�ô��� D����������
��3������ȼ�ϵ�ظ����ų���������Ҫ��___ __��
�õ�������ĵ缫��ӦΪ_ _ __��
��4������ȼ�ϵ�صĵ缫�϶��˲��ۣ���������Ŀ�ģ��������õĵ��������⣬���߱��������� ��
��5�����忴����������ϵ������������CxHy������ķ�Ӧ������CxHyΪ���飬��
��֪�����ȼ����Ϊ5 518 kJ·mol��1����д������ȼ���ȵ��Ȼ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
COCl2(g)  CO(g) + Cl2(g) ��H > 0������Ӧ�ﵽƽ��ʱ���ı�һ�ַ�Ӧ����������ʾ��ͼ��ȷ����
CO(g) + Cl2(g) ��H > 0������Ӧ�ﵽƽ��ʱ���ı�һ�ַ�Ӧ����������ʾ��ͼ��ȷ����
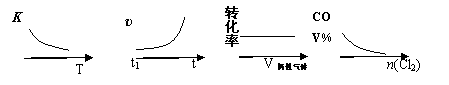
�� �� �� ��
A���ٱ�ʾ���¶����ߣ�ƽ�ⳣ���ı仯
B���ڱ�ʾ�����������Ӧ������ʱ��ı仯
C���۱�ʾ��ѹ�����£���Ӧ���ת��������������������ı仯
D���ܱ�ʾCO��������������Cl2���ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
SiCl4��������Ϊ��ɫҺ�壬�ӷ�����ǿ�ҵĴ̼��ԡ���SiCl4��ת��ΪSiHCl3���پ�������ԭ���ɸߴ��衣һ�������£���20L�����ܱ������з���SiCl4ת��ΪSiHCl3 �ķ�Ӧ��3SiCl4(g)��2H2(g)��Si(s) 4SiHCl3(g)����H��Q kJ·mol��1��2 min��ﵽƽ�⣬H2��SiHCl3�����ʵ���Ũ�ȷֱ�Ϊ0.1 mol·L��1��0.2 mol·L��1��
4SiHCl3(g)����H��Q kJ·mol��1��2 min��ﵽƽ�⣬H2��SiHCl3�����ʵ���Ũ�ȷֱ�Ϊ0.1 mol·L��1��0.2 mol·L��1��
��1���ӷ�Ӧ��ʼ��ƽ�⣬v(SiCl4)�� ��
��2���÷�Ӧ��ƽ�ⳣ������ʽΪK�� ���¶����ߣ�Kֵ������Q 0(�����������������)��
 ��3����ƽ������������г�������ʼʱ������SiCl4��H2(����Si����)������Ӧ�ٴδﵽƽ��ʱ����ԭƽ����Ƚϣ�H2����������� (���������С�����䡱)��
��3����ƽ������������г�������ʼʱ������SiCl4��H2(����Si����)������Ӧ�ٴδﵽƽ��ʱ����ԭƽ����Ƚϣ�H2����������� (���������С�����䡱)��
��4��ԭ�����У�ͨ��H2�����(��״����)Ϊ ��
��5��ƽ��������������Ϊ10 L���ٴδﵽƽ��ʱ��
H2�����ʵ���Ũ�ȷ�ΧΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ʳ�ؽ����λ������ж������д�ʩ�в��������ⶾ����(����)
A�������������� B�����ö���
C���ȴ���ţ�� D�����ο�ˮ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com