
 2Fe3O4(S)+C.
2Fe3O4(S)+C.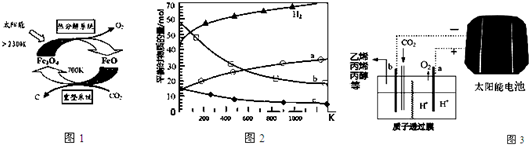
 .
.分析 (1)①该反应中Fe元素化合价由+3价变为+2价,O元素化合价由-2价变为0价,根据转移电子和Fe3O4之间的关系式计算;
②根据图知,反应物是二氧化碳和FeO,生成物的四氧化三铁和C,反应条件是700K;(2)①根据图知,升高温度,氢气物质的量增大,说明平衡逆向移动,则正反应是放热反应;a曲线随着温度升高,物质的量增大,为二氧化碳,b、c随着温度升高其物质的量降低,为生成物水、乙烯,但水的变化量大于乙烯,据此判断b曲线代表物质;
②压强之比等于其物质的量之比,设反应前氢气、二氧化碳物质的量分别是3xmol、xmol,反应后混合气体物质的量=$\frac{(3x+x)mol}{0.1MPa}×0.08MPa$=3.2xmol,反应平衡是气体物质的量减少量=(3x+x-3.2x)mol=0.8xmol,设二氧化碳参加反应的物质的量为ymol,
2CO2(g)+6H2(g)?C2H4(g)+4H2O(g)减少
2mol 3mol
ymol 0.8xmol
则:2mol:3mol=ymol:0.8xmol,解得y=$\frac{1.6x}{3}$,进而计算二氧化碳转化率;
C、O原子之间通过共用电子对形成二氧化碳共价化合物;
(3)①太阳能电池中光能转化为电能,电解强酸性的二氧化碳水溶液得到乙烯,电能转化为化学能;
②电解时,二氧化碳在b极上得电子发生还原反应生成乙烯.
解答 解:(1)①该反应中Fe元素化合价由+3价变为+2价,O元素化合价由-2价变为0价,分解2mol四氧化三铁转移4mol电子,则分解1mol四氧化三铁转移2mol电子,转移电子个数为2NA或1.204×1024,故答案为:2NA或1.204×1024;
②根据图知,反应物是二氧化碳和FeO,生成物的四氧化三铁和C,反应条件是700K,反应方程式为6FeO(S)+CO2 2Fe3O4(S)+C,
2Fe3O4(S)+C,
故答案为:6FeO(S)+CO2 2Fe3O4(S)+C;
2Fe3O4(S)+C;
(2)①根据图知,升高温度,氢气物质的量增大,说明平衡逆向移动,则正反应是放热反应;a曲线随着温度升高,物质的量增大,为二氧化碳,b、c随着温度升高其物质的量降低,为生成物水、乙烯,但水的变化量大于乙烯,所以b曲线代表H2O,故答案为:H2O;
②压强之比等于其物质的量之比,设反应前氢气、二氧化碳物质的量分别是3xmol、xmol,反应后混合气体物质的量=$\frac{(3x+x)mol}{0.1MPa}×0.08MPa$=3.2xmol,反应平衡是气体物质的量减少量=(3x+x-3.2x)mol=0.8xmol,
设二氧化碳参加反应的物质的量为ymol,
2CO2(g)+6H2(g)?C2H4(g)+4H2O(g)减少
2mol 3mol
ymol 0.8xmol
则2mol:3mol=ymol:0.8xmol,解得y=$\frac{1.6x}{3}$,故二氧化碳转化率=$\frac{\frac{1.6x}{3}mol}{xmol}×100%$=53.3%;
C、O原子之间通过共用电子对形成二氧化碳共价化合物,其形成过程为 ,
,
故答案为:53.3%; ;
;
(3)①太阳能电池中光能转化为电能,电解强酸性的二氧化碳水溶液得到乙烯,电能转化为化学能,
故答案为:太阳能转化为电能、电能转化为化学能;
②电解时,二氧化碳在b极上得电子发生还原反应生成乙烯,电极反应式为2CO2+12H++12e-=C2H4+4H2O,
故答案为:2CO2+12H++12e-=C2H4+4H2O.
点评 本题考查原电池和电解池原理、化学平衡计算、氧化还原反应有关计算,为高频考点,注意四氧化三铁中Fe元素化合价,难点是电极反应式的书写,题目难度不大.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案科目:高中化学 来源: 题型:解答题
 实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图所示).
实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图所示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KMnO4溶液、FeCl3溶液 | B. | 溴水、KMnO4溶液 | ||
| C. | NaOH溶液、FeCl3溶液 | D. | 溴水、Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数$\frac{{{k}_{1}}^{2}}{{k}_{2}}$ | |
| B. | 平衡后c(Cl2)=2.5×10-2mol•L-1 | |
| C. | 其他条件保持不变,反应在恒压条件下进行,则平衡常数K2增大 | |
| D. | 平衡时NO2的转化率为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HA是弱酸 | B. | HA的电离方程式为HA═H++A- | ||
| C. | 该溶液中c(HA)+c(A-)=0.1 mol•L-l | D. | NaA溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸具有强氧化性,但SO2气体可以用浓硫酸干燥 | |
| B. | 常温下实验室可以用稀硝酸与铁反应制取NO气体 | |
| C. | 王水溶解金的过程为氧化还原反应,还原产物为NO2 | |
| D. | SiO2不仅能与氢氧化钠溶液反应,也能与氢氟酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com