
������ʵ������ó��Ľ�����ȷ����
ѡ�� | ʵ����������� | ʵ����� |
A | ��ij��Һ��ͬʱ�μӼ���KSCN��Һ��������������ˮ����Һ���Ѫ��ɫ | ����Һ��һ������Fe2+ |
B | ������ʯ��ˮ������ܻ���Na2CO3��NaHCO3��Һ�У����ְ�ɫ���� | ����Һ��һ������Na2CO3 |
C | �����£���pH�ƲⶨijŨ��NaHSO3��Һ��pHԼΪ5.20 | ����Һ�е�HSO3-�ĵ���̶ȴ�������ˮ��̶� |
D | �����£���ij��Һ�еμ�ϡNaOH��Һ����ʪ��ĺ�ʯ����ֽ�����Թܿڣ���ֽ������ | ����Һ��һ��������NH4+ |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶��϶����¿���ѧ�Ծ��������棩 ���ͣ������
��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g)+3H2(g) CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й����������ı仯��
CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й����������ı仯��
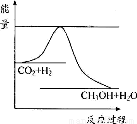
��1�����ڸ÷�Ӧ������˵���У���ȷ����_______��
A����H>0����S>0�� B����H>0����S<0��
C����H<0����S<0�� D����H<0����S>0��
��2����ͼ����������ߵ����͵�֮��IJ�ֵ����
��3����CH4��H2OΪԭ�ϣ�ͨ�����з�Ӧ���Ʊ��״���
��CH4(g)+H2O(g) == CO(g)+3H2(g) ��H=+206.0KJ/mol
��CO(g) + 2H2(g) = CH3OH(g) ��H=-129.0KJ/mol
CH4(g)��H2O(g)��Ӧ����CH3OH(g)��H2(g)���Ȼ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��������Ϫ��һ��ѧ������ѧ�����п�������ѧ�Ծ��������棩 ���ͣ�ѡ����
�ݱ�������ѧ�ҷ��������·�Ӧ��O2+PtF6��O2��PtF6 ������֪O2��PtF6��Ϊ���ӻ��������PtΪ+5�ۣ����ڴ˷�Ӧ������˵����ȷ���ǣ� ��
������֪O2��PtF6��Ϊ���ӻ��������PtΪ+5�ۣ����ڴ˷�Ӧ������˵����ȷ���ǣ� ��
A���˷�Ӧ�Ƿ�������ԭ��Ӧ
B��O2��PtF6�� ����Ԫ�صĻ��ϼ���+1��
C���ڴ˷�Ӧ�У�O2����������PtF6�ǻ�ԭ��
D���˷�Ӧ�У�ÿ����1mol O2��PtF6��ת��1mol ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪�ֳ��������ѧУ�����ϵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ����٤��������ֵ������˵������ȷ����
A�����³�ѹ�£�11.2L��NO2��CO2������庬��NA��Oԭ��
B����״���£�22.4L����ϩ�к��еĹ��õ��Ӷ���Ϊ12NA
C��1L0.1mol��L��1�İ�ˮ�к���0.1NA��OH?
D����ʯīΪ�缫����Ȼ�ͭ��Һʱ����������ʧȥ����NA������������������32g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ���������ʵ�ѭ�������ж��֣����磺
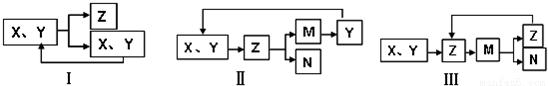
���б�ʾ����ȷ����
A��ͼ��ɱ�ʾ�ϳɰ�������N2��H2��ѭ��ʹ��
B��ͼ��ɱ�ʾ������ڵ�MgCl2�õ�þ������HClѭ��ʹ��
C��ͼ��ɱ�ʾ���������������ᣬ����NOѭ��ʹ��
D��ͼ������ں����ƴ���CO2��ѭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������������ѧ��һ��10�»�ѧ���������棩 ���ͣ�������
��1��Nԭ�ӵ�Ħ��������_________��1mol HNO3��������____________�� 1mol HNO3Լ����_________________����ԭ��.
��2����״����11.2L HCl��������ʵ�����______________,����HCl���� ����ˮ�����1L��Һ,����������Һ�����ʵ���Ũ����____________________.
��3��2mol OH? Լ����___________________������.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ������ѧ��12�µ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��������Ϊa��ij���ʵ���Һmg����������Ϊb�ĸ����ʵ���Һng��Ϻ�������pgˮ���õ�����Һÿ��������Ϊqg�����ʵ���Ũ��Ϊc�������ʵķ���������Է���������Ϊ( )
A��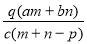 B��
B��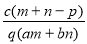 C��
C��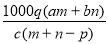 D��
D��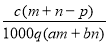
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��д��ȷ����
A�� Na2O ����ˮ��Na20+ H2O=2Na+ + 20H��
B���� Ca(C10)2 ��Һ��ͨ����� C02 �� 2C10-+H20+C02=2HC1O+CO32-
C����FeC13��Һ��ʴͭ�壺Fe3ʮʮCu=Fe2ʮʮCu2ʮ
D��̼�������ϡ����:CaCO3+2H+=Ca2++CO2 +H20
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ�����ϵ�����ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ���ǣ� ��
A����֪�����ۻ���Ϊ6.0 kJ�qmol-1�������������Ϊ20 kJ�qmol-1������1mol������2mol��������ۻ�����ȫ���ڴ��Ʊ�������������ֻ���ƻ�����30%�����
B����֪һ���¶��£�������Һ�����ʵ���Ũ��Ϊc�������Ϊa��K a��(ca)2/C(1?a)������������CH3COONa���壬�����ƽ��CH3COOH CH3COO-+H+�����ƶ���a��С��Ka����
CH3COO-+H+�����ƶ���a��С��Ka����
C�����û����飨l��������ϩ��l���ͱ���l���ı�ȼ���ȷֱ�Ϊ-3916kJ��mol-1��-3747 kJ��mol-1��-3265kJ��mol-1����֤���ڱ������в����ڶ�����̼̼˫��
D�������к��ȷ�Ӧ�У���������¶ȼ��ϵ�����ˮ��ϴ������ô����cm��t����õ���Q�����ƫС
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com