
.实验室用50mL浓盐酸跟足量的氯酸钾固体共热制取氯气,反应的化学方程式为:KClO3+6HCl(浓) KCl+3Cl2↑+3H2O.(只第(3)题写计算过程)
KCl+3Cl2↑+3H2O.(只第(3)题写计算过程)
(1)浓盐酸在反应中显示出来的性质是 (填写编号).
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)若产生0.1mol Cl2,则转移电子的物质的量为 mol.
(3)若反应中HCl的利用率只有50%,当反应结束时,生成Cl20.15mol,求浓盐酸的物质的量浓度.(写计算过程)
考点:化学方程式的有关计算.
分析:(1)HCl中Cl元素的化合价由﹣1价升高0,则HCl具有还原性,又生成盐KCl,则表现酸的酸性;
(2)根据氯气物质的量计算KClO3的物质的量,KClO3中Cl元素的化合价由+5价降低0,据此计算转移电子;
(3)根据氯气物质的量计算参加反应HCl的物质的量,再根据HCl利用率计算盐酸中HCl总物质的量,根据c=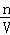 计算盐酸物质的量浓度.
计算盐酸物质的量浓度.
解答: 解:(1)在反应KClO3+6HCl(浓) KCl+3Cl2↑+3H2O中,HCl中Cl元素的化合价由﹣1价升高0,则HCl具有还原性,又生成盐KCl,则表现酸的酸性,
KCl+3Cl2↑+3H2O中,HCl中Cl元素的化合价由﹣1价升高0,则HCl具有还原性,又生成盐KCl,则表现酸的酸性,
故答案为:②;
(2)产生0.1mol Cl2,根据KClO3+6HCl(浓) KCl+3Cl2↑+3H2O,可知反应的KClO3的物质的量为
KCl+3Cl2↑+3H2O,可知反应的KClO3的物质的量为 ,KClO3中Cl元素的化合价由+5价降低0,转移电子物质的量为
,KClO3中Cl元素的化合价由+5价降低0,转移电子物质的量为 ×5=
×5=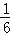 mol,
mol,
故答案为: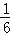 ;
;
(3)生成Cl20.15mol,根据KClO3+6HCl(浓) KCl+3Cl2↑+3H2O,可知反应的HCl的物质的量为0.15mol×
KCl+3Cl2↑+3H2O,可知反应的HCl的物质的量为0.15mol× =0.3mol,HCl的利用率只有50%,则盐酸中HCl总物质的量为
=0.3mol,HCl的利用率只有50%,则盐酸中HCl总物质的量为 =0.6mol,故盐酸物质的量浓度为
=0.6mol,故盐酸物质的量浓度为 =12mol/L,
=12mol/L,
答:浓盐酸的物质的量浓度为12mol/L.
点评:本题考查氧化还原反应、化学方程式有关计算,比较基础,侧重对基础知识的巩固.


科目:高中化学 来源: 题型:
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是()

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e﹣=Cu
C. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D. a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
把含硫40%的硫铁矿先制成硫酸,再吸收氨气制成硫酸铵.1t这种硫铁矿在理论上能制得硫酸铵( )
|
| A. | 2.26 t | B. | 1.98 t | C. | 1.65 t | D. | 1.06 t |
查看答案和解析>>
科目:高中化学 来源: 题型:
能用H++OH﹣=H2O来表示的化学反应是( )
A.氢氧化镁和稀盐酸反应 B.Ba(OH)2溶液滴入稀硫酸中
C.澄清石灰水和稀硝酸反应 D.二氧化碳通入澄清石灰水中
查看答案和解析>>
科目:高中化学 来源: 题型:
组成中有氢氧根的盐叫做碱式盐,酸根中含有氢元素的盐叫做酸式盐.下列盐中,既不是碱式盐又不是酸式盐的是( )
|
| A. | KHSO4 | B. | NH4NO3 | C. | Ca(H2PO4)2 | D. | Cu2(OH)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
|
| A. | 化学反应一定是放热反应 |
|
| B. | 反应物的总能量小于生成物的总能量的化学反应是放热反应 |
|
| C. | 化学反应中能量变化的大小与反应物的质量多少无关 |
|
| D. | 能量变化是化学反应的基本特征之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铁氧磁体法处理含Cr2O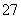 的废水的原理如下:向含
的废水的原理如下:向含
Cr2O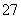 的酸性废水中加入FeSO4·7H2O,将Cr2O
的酸性废水中加入FeSO4·7H2O,将Cr2O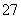 还原为Cr3+,调节溶液的pH,使铁、铬元素转化为组成
还原为Cr3+,调节溶液的pH,使铁、铬元素转化为组成
相当于FeⅡ[Fe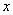 ·Cr
·Cr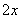 ]O4(铁氧磁体,罗马数字表示元素的价态)的沉淀。处理含1 mol Cr2O
]O4(铁氧磁体,罗马数字表示元素的价态)的沉淀。处理含1 mol Cr2O 的废水至少需要
的废水至少需要
加入a mol FeSO4·7H2O。下列结论正确的是 ( )
A.x=0.5,a=8 B.x=0.5,a=10 C.x=1.5,a=8 D.x=1.5,a=10
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
 A.碳酸氢铵溶液与过量的氢氧化钠溶液反应 H+ + OH — H2O
A.碳酸氢铵溶液与过量的氢氧化钠溶液反应 H+ + OH — H2O
B.氢氧化铝与足量盐酸反应 Al(OH)3+3H+ ═ Al3++3H2O
 C.钠和冷水反 Na+2H2O N
C.钠和冷水反 Na+2H2O N a++H2↑+OH—
a++H2↑+OH—
 D.铜片与稀硝酸反应 Cu+NO3—+4H+ Cu2++NO↑+2H2O
D.铜片与稀硝酸反应 Cu+NO3—+4H+ Cu2++NO↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com