(2009?安徽模拟)A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素原子的电子层数为n,最外层电子数为2n+1,A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物.回答下列问题:
(1)写出下列各元素的名称:A
氢
氢
D
氧
氧
(2)上述五种元素中,第一电离能最小的元素是
Na
Na
,基态原子未成对电子数最多的原子核外电子排布式为
1s22s22p3
1s22s22p3
.
(3)已知:BA
3DA(g)+A
2D(g)=BD
2(g)+3A
2(g)△H
1=+49.0kJ/mol,BA
3DA(g)+1/2D
2(g)=BD
2(g)+2A
2(g)△H
2=-192.9kJ/mol,试写出:气态BA
3DA完全燃烧生成气态A
2D的热化学方程式(用推出的元素符号书写);
CH
3OH(g)+
O
2(g)=CO
2(g)+2H
2O(l)△H=-676.7kJ/mol
CH
3OH(g)+
O
2(g)=CO
2(g)+2H
2O(l)△H=-676.7kJ/mol
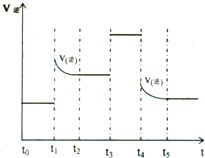
(4)对可逆反应3A
2(g)+C
2(g)?2CA
3(g)当反应达到平衡位置时不断改变条件(不改变A
2、C
2和CA
3的量),右图表示反应速率与反应过程的关系,其中表示平衡混合物中CA
3的含量最高的一段时间是
t0-t1
t0-t1
.在一定温度下,若将4amol A
2和2a mol C
2放入lL的密闭容器中,充分反应后测得C
2的转化率为50%,则该反应的平衡常数为
.若此时再向该容器中投入a mol A
2,a mol C
2利2a mol CA
3,判断平衡移动方向
正
正
(“正”“逆”或“不移动”).

 (2009?安徽模拟)A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素原子的电子层数为n,最外层电子数为2n+1,A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物.回答下列问题:
(2009?安徽模拟)A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素原子的电子层数为n,最外层电子数为2n+1,A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物.回答下列问题:

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案