
 某同学为了探究元素非金属性递变规律,设计了如图所示实验装置.
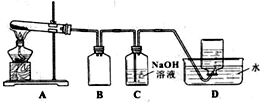
某同学为了探究元素非金属性递变规律,设计了如图所示实验装置.分析 (1)元素的非金属性越强,其最高价氧化物的水化物酸性越强、其单质的氧化性越强,根据信息需根据强酸制弱酸的原理探究元素非金属性递变规律:元素非金属性与对应最高价含氧酸之间的关系如图装置来一次性完成,C、N属于同一周期,C、Si属于同一主族,C、N、Si三种非金属元素的非金属性强弱比较,第一支试管中反应是碳酸钙和稀硝酸反应生成二氧化碳,证明氮非金属性大于碳,饱和碳酸氢钠的作用是除去二氧化碳中硝酸蒸气,第三支试管中二氧化碳和硅酸钠反应,证明碳非金属性大于硅;
(2)第一支试管中反应是碳酸钙和稀硝酸反应生成二氧化碳,第三支试管中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,证明碳的非金属性大于硅,饱和碳酸氢钠的作用是除去二氧化碳中硝酸蒸气,据此分析观察到的现象;
(3)根据最高价氧化物的水化物酸性越强,其元素的非金属性越强判断.
解答 解:(1)同周期自左而右,核电荷数增大,原子半径减小,原子核对电子吸引增强,失去电子能力减弱,获得电子的能力增强,故同周期从左到右,金属性逐渐减弱,非金属性逐渐增强,同主族元素从上到下元素的金属性逐渐增强,非金属性逐渐减弱,C、N、Si三种非金属,C、N属于同一周期,C、Si属于同一主族,推知C、N、Si三种元素非金属性的强弱为N>C>Si,根据信息需根据强酸制弱酸的原理探究元素非金属性递变规律:第一支试管装置用来制取二氧化碳,故a为稀硝酸,c为碳酸钙,碳酸钙和稀硝酸反应生成二氧化碳,证明氮非金属性大于碳,硝酸易挥发,故饱和碳酸氢钠的作用是除去二氧化碳中硝酸,第三支试管中为硅酸钠溶液,证明碳非金属性大于硅,
故答案为:稀硝酸;碳酸钙;硅酸钠溶液;
(2)第一支试管中反应是碳酸钙和稀硝酸反应生成二氧化碳,证明氮非金属性大于碳,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,c为碳酸钙,可观察到c产生气泡,碳酸钙溶解,第三支试管中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,证明碳的非金属性大于硅,d装置中观察到溶液变浑浊,饱和碳酸氢钠的作用是除去二氧化碳中硝酸,
故答案为:产生气泡,碳酸钙溶解;产生白色沉淀;
(3)最高价氧化物的水化物酸性越强,其元素的非金属性越强,酸性:硝酸>碳酸>硅酸,则非金属性:N>C>Si;
故答案为:N>C>Si.
点评 本题将元素及其化合物、元素周期律与实验知识结合起来,考查了审题能力、思维能力,具有较强的综合性,注意实验设计的原理和方法,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | c(H+) | B. | H+个数 | C. | CH3COOH分子数 | D. | c(H+)/c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁跟稀盐酸反应2Fe+6H+═2Fe3++3H2↑ | |
| B. | 盐酸中加入碳酸钙CO32-+2H+═H2O+CO2↑ | |
| C. | CO2通入足量澄清石灰水中CO2+Ca2++2OH-═CaCO3↓+H2O | |
| D. | NaHCO3溶液中加入盐酸CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 工业合成氨原理N2(g)+3H2(g)?2NH3(g)△H<0.在一定条件下达化学平衡后,在t时突然改变条件,反应速率的变化如右图所示,则t时所改变的条件是( )
工业合成氨原理N2(g)+3H2(g)?2NH3(g)△H<0.在一定条件下达化学平衡后,在t时突然改变条件,反应速率的变化如右图所示,则t时所改变的条件是( )| A. | 增大压强 | B. | 降低温度 | C. | 升高温度 | D. | 分离出氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 为了探究AgNO3的氧化性和热稳定性,某化学兴趣小组设计了如下实验.
为了探究AgNO3的氧化性和热稳定性,某化学兴趣小组设计了如下实验.| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | ① | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入 ②,振荡 | ③ | 存在Fe2+ |
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com