
【题目】下列有关物质性质的叙述错误的是
A.HNO3受热分解可生成NO2
B.Na在O2中燃烧可生成Na2O2
C.CaCl2暴露在空气中可生成CaCO3
D.向FeCl3溶液中滴加KSCN溶液,溶液显红色
科目:高中化学 来源: 题型:
【题目】《本草纲目》中的“石碱”条目下写道:“采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面。”下列说法错误的是( )
A.“石碱”中含有离子键B.“石碱”中含有非极性共价键
C.“石碱”是离子化合物D.“石碱”中含有极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b两个极易导热的密闭容器,a保持容积不变,b中的活塞可上下移动,以保持内外压强相等.在相同条件下将3molA、1molB分别同时混合于a、b两容器中,发生反应:
3A(g)+B(g)2C(g)+D(g)
(1)达平衡时,a中A的浓度为M molL﹣1 , C的浓度为N molL﹣1 , b中A的浓度为m molL﹣1 , C的浓度为n molL﹣1 , 则Mm;Nn; (填“>”或“<”或“=”或“无法比较”)
(2)保持温度不变,按下列配比分别充入 a、b 两容器,达平衡后a中C的浓度为N molL﹣1的是 , b中C的浓度为n molL﹣1的是
A.6molA+2molB B.3molA+2molC C.2molC+1molB+1mol D
D.2molC+1molD E.1.5molA+0.5molB+1molC+0.5molD
(3)若将2molC和2molD充入a中,保持温度不变,平衡时A的浓度为WmolL﹣1 , C的浓度为YmolL﹣1 , 则W和M,Y和N之间的关系为WM、YN. (填>、<、=、无法比较)
(4)保持温度不变,若将4molC和2molD充入a中,平衡时A的浓度为R molL﹣1 , 则关系式正确的是
A.R=2M
B.R<M
C.M<R<2M
D.R>2M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知NaHA水溶液呈碱性。
①用离子方程式表示NaHA水溶液呈碱性的原因:______________________________。
②在NaHA水溶液中各离子浓度的大小关系是:______________________________。
(2)25℃,两种酸的电离平衡常数如表.
Ka1 | Ka2 | |
H2SO3 | 1.3×10﹣2 | 6.3×10﹣8 |
H2CO3 | 4.2×10﹣7 | 5.6×10﹣11 |
①HSO3﹣的电离平衡常数表达式K=______。
②H 2SO3溶液和NaHCO3溶液反应的主要离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法与社会可持续发展理念相符合的是
A.推广一次性塑料袋的使用
B.应用高效洁净的能源转换技术
C.加快化石燃料的开采与使用
D.大量开采地下水以满足工业生产需求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是
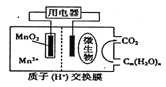
A. 正极反应式为MnO2+4H++2e-===Mn2++2H2O
B. 微生物所在电极区放电时发生还原反应
C. 放电过程中,H+从正极区移向负极区
D. 若用该电池给铅蓄电池充电,MnO2电极质量减少8.7g,则铅蓄电池阴极增重9.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,有关说法正确的是
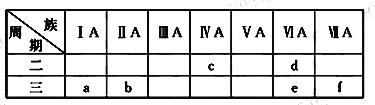
A. e的氢化物比d的氢化物稳定
B. a、b、e三种元素的原子半径:e>b>a
C. c、e、f的最高价氧化物对应的水化物的酸性依次增强
D. 六种元素中,c元素单质的化学性质最活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势如图所示: 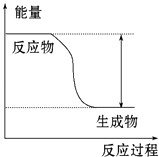
(1)该反应为反应(填“吸热”或“放热”).
(2)若要使该反应的反应速率加快,下列措施可行的是(填字母).
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为(填“正”或“负”)极.铜片上的现象为该极上发生的电极反应为 , 外电路中电子由极(填“正”或“负”,下同)向极移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法正确的是( )
A.3.55gCl2通入足量水中充分反应,转移电子数为0.05NA
B.18gNH4+含有质子数为10NA
C.13.8gNO2与足量水反应时,转移电子的数目为0.2NA
D.标准状况下,相同体积的SO3、HCl、NO含有的分子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com