
| A. | 3.2 | B. | 0.2 | C. | $\frac{1}{180}$ | D. | $\frac{4}{45}$ |
分析 反应①的平衡常数k=$\frac{{c}^{2}({N}_{2}{O}_{4})×c({O}_{2})}{{c}^{2}({N}_{2}{O}_{5})}$,N2O5分解得到N2O4部分转化为NO2(g),平衡时c(O2)=0.2mol•L-1,c(NO2)=0.6mol•L-1,则平衡时c(N2O4)=2c(O2)-$\frac{1}{2}$c(NO2),平衡时c(N2O5)=$\frac{1mol}{2L}$-2c(O2),代入平衡常数表达式计算.
解答 解:N2O5分解得到N2O4部分转化为NO2(g),平衡时c(O2)=0.2mol•L-1,c(NO2)=0.6mol•L-1,则:
平衡时c(N2O4)=2c(O2)-$\frac{1}{2}$c(NO2)=0.2mol/L×2-$\frac{1}{2}$×0.6mol/L=0.1mol/L,
平衡时c(N2O5)=$\frac{1mol}{2L}$-2c(O2)=0.5mol/L-0.2mol/L×2=0.1mol/L,
故反应①的平衡常数k=$\frac{{c}^{2}({N}_{2}{O}_{4})×c({O}_{2})}{{c}^{2}({N}_{2}{O}_{5})}$=$\frac{0.{1}^{2}×0.2}{0.{1}^{2}}$=0.2,
故选B.
点评 本题考查化学平衡常数计算,关键是计算平衡时c(N2O4),难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 用碱式滴定管盛装高锰酸钾溶液 | B. | 用铁坩埚灼烧烧碱 | ||
| C. | 用铁坩埚除去纯碱晶体中的结晶水 | D. | 加热蒸发皿时不用石棉网 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度相同的溶液中所含溶质的微粒数相同 | |
| B. | 常温常压下,0.1molH2气体约含6.02×1022个H2分子 | |
| C. | 1mol•L-1醋酸溶液100mL中H+的个数约为0.1NA | |
| D. | 标准状况下,1molH2O的体积约22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标况下,11.2L SO3所含的分子数目为0.5 NA | |
| B. | 1L0.1 mol•L-1的碳酸氢钠溶液中含碳酸氢根离子数为0.1NA | |
| C. | 常温常压下,1.7gH2O2中含有的电子数为0.9nA | |
| D. | 8 Al+3 NH4ClO4═4 Al2O3+3NH3+3HCl 反应中,消耗27gAl粉时,转移的电子数目为2.75NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
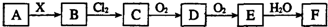
| A. | 当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4 | |
| B. | 当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3 | |
| C. | B和Cl2的反应是氧化还原反应 | |
| D. | 当X是强酸时,C在常温下是气态单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、M两种元素只能形成X2M型化合物 | |
| B. | 元素Y、Z、W的单质晶体属于同种类型的晶体 | |
| C. | 元素W和M的某些单质可作为水处理中的消毒剂 | |
| D. | 由于W、Z元素的氢气化物还原性:W>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn和Cu | B. | Al和Fe | C. | Ag和Zn | D. | Mg和Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na+的基态电子排布图是: | |
| B. | 7.8 gNa2S和7.8 gNa2O2中含有的阴离子数目均为0.1NA | |
| C. | Na2S的电子式: | |
| D. | 氯离子结构示意图为: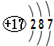 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com