
| A. | Ag+、Cu2+、Sb3+ | B. | Cu2+、Ag+、Sb3+ | C. | Sb3+、Ag+、Cu2+ | D. | Ag+、Sb3+、Cu2+ |
分析 向该溶液中逐滴加入0.010mol•L-1的Na2S溶液时,c(S2-)=0.01mol/L,结合Ksp计算阳离子的浓度,阳离子的浓度小的先沉淀,以此来解答.
解答 解:向该溶液中逐滴加入0.010mol•L-1的Na2S溶液时,c(S2-)=0.01mol/L,由Ksp可知,生成沉淀时c(Ag+)=$\sqrt{\frac{1.6×1{0}^{-49}}{0.01}}$=4.0×10-25mol/L,c(Cu2+)=$\frac{8.9×1{0}^{-35}}{0.01}$=8.9×10-33mol/L,c(Sb3+)=$\sqrt{\frac{1.0×1{0}^{-30}}{(0.01)^{3}}}$=1.0×10-12mol/L,则三种阳离子产生沉淀的先后顺序为Cu2+、Ag+、Sb3+,
故选B.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握Ksp的计算、离子沉淀的顺序为解答关键,侧重分析与计算能力的考查,注意Ksp与K的关系及应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
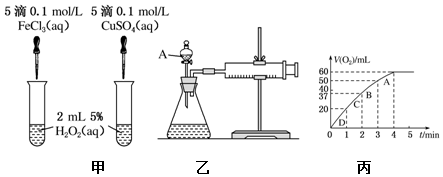
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,NH4+、Fe2+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,K+、Ag+、H+、NO3-可以大量共存 | |
| C. | 向该溶液中通入SO2气体,反应的离子方程式为SO2+3CIO-+H2O═SO42-+CI-+2HCIO | |
| D. | 向该溶液中加入浓盐酸,反应的离子方程式为CIO-+CI-+2H+═Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.08g镁铝合金中含有镁和铝的质量分别为1.92g、2.16g | |
| B. | 生成沉淀的最大质量为10.88g | |
| C. | 若白色沉淀只有Mg(OH)2,该NaOH溶液的浓度至少为0.96mol/L | |
| D. | 溶解4.08 g镁铝合金时,剩余盐酸的物质的量为0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
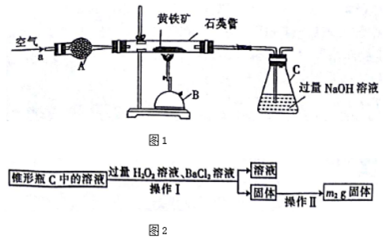
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com