


科目:高中化学 来源:不详 题型:计算题
 N2O3(g)+O2(g),②N2O3(g)
N2O3(g)+O2(g),②N2O3(g) N2O(g)+O2(g),在1 L密闭容器中充入4 mol N2O5,加热到t ℃,达到平衡状态后O2的平衡浓度为4.5 mol·L-1,N2O3的平衡浓度为1.62 mol·L-1,求N2O5和N2O的平衡浓度。
N2O(g)+O2(g),在1 L密闭容器中充入4 mol N2O5,加热到t ℃,达到平衡状态后O2的平衡浓度为4.5 mol·L-1,N2O3的平衡浓度为1.62 mol·L-1,求N2O5和N2O的平衡浓度。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2R(g)+W(g),反应达到平衡时,测知X和Y的转化率分别为25%和50%,则化学方程式中的n值为( )
2R(g)+W(g),反应达到平衡时,测知X和Y的转化率分别为25%和50%,则化学方程式中的n值为( )| A.4 | B.3 | C.2 | D.1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HI(g)达到平衡的标志是( )
2HI(g)达到平衡的标志是( )| A.压强不随时间的变化而变化 | B.混合气的平均相对分子质量一定 |
| C.生成n mol H2的同时生成2n mol HI | D.v(H2)=v(I2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
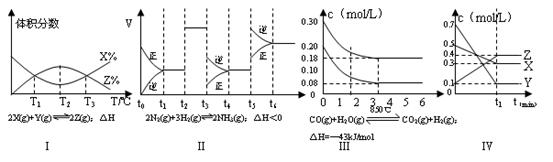
| A.由图象Ⅰ知,该反应在T1、T3处达到平衡,且该反应的△H<0 |
| B.由图象Ⅱ知,该反应在t5阶段NH3体积分数最大 |
| C.图象Ⅲ是在10L容器中850℃时反应,由图知,到4min时,反应放出51.6kJ的热量 |
| D.由图象Ⅳ知,相同条件下起始时投入0.3mol/LX、0.1mol/LY和0.4mol/LZ反应,达到平衡后,Z的浓度为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z
2Z| A.平衡常数K值越大,X的转化率越大 |
| B.达到平衡时,反应速率v正(X)==2v逆(Y) |
| C.达到平衡后,降低温度,正向反应速率减小的倍数小于逆向反应速率减小的倍数 |
| D.达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方法移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HI已达到平衡状态的是
2HI已达到平衡状态的是| A.一个H-H键断裂的同时有一个I-I键组成 |
| B.一个H-H键断裂的同时有一个I-I键断裂 |
| C.一个H-I键形成的同时有一个H-H键断裂 |
| D.一个H-I键断裂的同时有一个H-H键形成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等于1.369g/L |
| B.等于2.054g/L |
| C.在1.369g/L和2.054g/L之间 |
| D.大于2.054g/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com