
【题目】下列关于有机物结构、性质的说法正确的是
A. 石油的分馏、裂化和煤的干馏都是化学变化
B. 甲烷的一氯代物只有一种可证明甲烷分子呈正四面体形
C. 邻二甲苯只有一种结构,能证明苯环中不存在碳碳单键和碳碳双键交替的结构
D. 正丁烷和异丁烷的熔沸点相同,它们的一氯取代物都只有两种
【答案】C
【解析】
A.石油的分馏属于物理变化,错误;
B.甲烷若为正方形结构,其一氯代物只有一种,故甲烷的一氯代物只有一种无法证明甲烷分子呈正四面体形;二氯甲烷只有一种可证明甲烷分子呈正四面体形,错误;
C.若苯环中存在碳碳单键和碳碳双键交替的结构,则邻二甲苯有 、
、 两种结构,但实际上邻二甲苯只有一种结构,故能证明苯环中不存在碳碳单键和碳碳双键交替的结构,正确;
两种结构,但实际上邻二甲苯只有一种结构,故能证明苯环中不存在碳碳单键和碳碳双键交替的结构,正确;
D. 同分异构体,支链越多,熔、沸点越低(高度对称结构除外),故正丁烷的熔沸点比异丁烷高,错误;
物质变化 | 物理变化 | 化学变化 |
三馏 | 蒸馏、分馏 | 干馏 |
四色 | 焰色反应 | 显色反应、颜色反应、指示剂变色反应 |
五解 | 潮解 | 分解、电解、水解、裂解 |
十八化 | 熔化、汽化、液化、酸化 | 氢化、氧化、水化、风化、炭化、钝化、催化、皂化、歧化、卤化、硝化、酯化、裂化、油脂的硬化 |


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】按要求写出下列方程式:
(1)硫酸铝的电离方程式:___。
(2)BaCO3与稀盐酸溶液反应的化学方程式:____。
(3)实验室制氯气的化学方程式:____。
(4)写出工业制漂白粉的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 反应 2Mg+CO2 ![]() 2MgO+C△H<0 从熵变角度看,可自发进行
2MgO+C△H<0 从熵变角度看,可自发进行
B. 在密闭容器发生可逆反应:2NO(g)+2CO(g)N2(g)+2CO2(g)△H=-113.0kJ/mol,达到平衡后,保持温度不变,缩小容器体积,重新达到平衡后,△H 变小
C. 根据 HClO 的 Ka=3.0×108,H2CO3 的 Ka1=4.3×107,Ka2=5.6×1011,可推测相同状况 下,等浓度的 NaClO 与 Na2CO3 溶液中,pH 前者小于后者
D. 已知:Ksp(AgCl)=1.8×1010,Ksp(Ag2CrO4)=2.0×1012,将等体积浓度为1.0×10﹣4mol/L 的 AgNO3 溶液滴入到浓度均为 1.0×10﹣4mol/L 的 KCl 和 K2CrO4 的混合溶液中产生两种不同沉淀,且 Ag2CrO4 沉淀先产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3 作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的 催化剂研究曾被列入国家 863 计划。
(1)催化剂常具有较强的选择性,即专一性。已知:反应 I :4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g)△H= 905.0 kJ·mol-1 反应 II : 4NH3(g)+3O2(g)
4NO(g) +6H2O(g)△H= 905.0 kJ·mol-1 反应 II : 4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H= 1266.6 kJ·mol-1 写出 NO 分解生成 N2 与 O2 的热化学方程式_________。
2N2(g) +6H2O(g) △H= 1266.6 kJ·mol-1 写出 NO 分解生成 N2 与 O2 的热化学方程式_________。
(2)在恒温恒容装置中充入一定量的 NH3 和 O2,在某催化剂的作用下进行反应 I ,测得不同时 间的 NH3 和 O2,的浓度如下表:
时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
c(NH3)/mol·L1 | 1.00 | 0.36 | 0.12 | 0.08 | 0.072 | 0.072 |
c(O2)/mol L1 | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
则下列有关叙述中正确的是_____。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内 4v 正(NH3) =6v 逆(H2O)时,说明反应已达平衡
C.当容器内n(NO)/n(NH3)=1 时,说明反应已达平衡
D.前 10 分钟内的平均速率 v( NO)=0.088 mol·L-1·min-1
(3)制备催化剂时常产生一定的废液,工业上常利用氢硫酸检测和除去废液中的 Cu2+。 已知:25℃时,K1(H2S) =1.3×107,K2(H2S) =7.1×1015,Ksp(CuS) =8.5×1045
①在计算溶液中的离子浓度时,涉及弱酸的电离通常要进行近似处理。则 0.lmol L1 氢硫 酸的 pH≈______(取近似整数)。
②某同学通过近似计算发现 0.lmol L1 氢硫酸与 0.0lmol L1 氢硫酸中的 c(S2)相等,而且 等于_____mol·L1
③已知,某废液接近于中性,若加入适量的氢硫酸,当废液中 c(Cu2+) >_____mol·L1(计算 结果保留两位有效数字),就会产生 CuS 沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项中所示的物质间转化均能实现的是
A. Ca(OH)2![]() Ca(ClO)2
Ca(ClO)2![]() HClO
HClO
B. SiO2![]() Na2SiO3
Na2SiO3![]() H2SiO3
H2SiO3
C. FeS2![]() SO2
SO2![]() (NH4)2SO4
(NH4)2SO4
D. 饱和NaCl溶液![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂空气充电电池有望成为电动汽车的实用储能设备。工作原理示意图如下,下列叙述正确的是
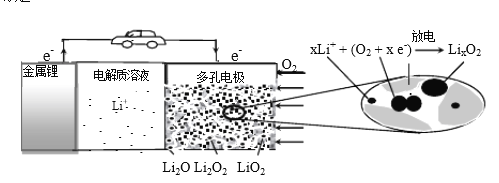
A. 该电池工作时Li+向负极移动
B. Li2SO4溶液可作该电池电解质溶液
C. 电池充电时间越长,电池中Li2O 含量越多
D. 电池工作时,正极可发生: 2Li+ +O2+ 2e-=Li2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。电解一段时间后,若在电解池中C极一侧出来的气体无色无味,D极一侧出来的气体呈黄绿色有刺激性气味。请回答以下问题:

(1)已知铅蓄电池在放电时发生的反应:Pb+PbO2+4H++2SO42-=2PbSO4+2H2O,则A极的电极反应为___________________________;
(2)电解饱和食盐水的离子反应方程式是__________________;
(3)电极C的电极反应是_____________________________________________;
(4)电解时为防止两种气体产物混合,用阳离子交换膜做隔膜。则电解时Na+从______极区移向_____极区(填“C”或“D”);
(5)若电路上有0.2mol电子的电量通过,则铅蓄电池中消耗硫酸_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(加试题)NH4Al(SO4)2·12H2O(铵明矾)可用作泡沫灭火器的内留剂、石油脱色剂等。某兴趣小组同学用氧化铁、铝粉、镁条和氯酸钾等物质做铝热反应后的铝灰及硫酸铵等为原料制备铵明矾的实验,步骤如下:
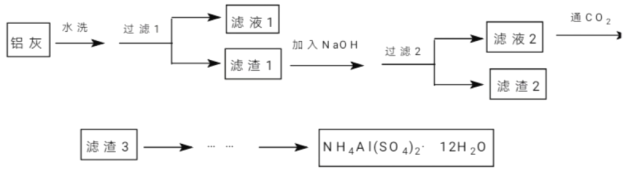
(1)下列有关说法中正确的是_________。
A.“滤液1”中含有K+、Mg2+、Cl-
B.“滤渣1”和“滤渣2”中含有相同的物质
C.“过滤1”可用倾析法,以缩减实验时间
D.将“滤液3”蒸干并灼烧,可得纯碱
(2)用NaOH溶解“滤渣1”时,可以采用_________的方式提高浸出率(写出3条)。
(3)向“滤液2”中通入足量的CO2,写出相应的离子反应方程式__________________。
(4)由“滤渣3”制备铵明矾,经过如下步骤:a→g→_________→h(依次填入正确的序号)
a.加硫酸溶解 b.抽滤
c.加入蒸发皿中
d.降温结晶
e.蒸发至表面出现晶膜
f.配制饱和硫酸铵溶液
g.将硫酸铝溶液转移至蒸发皿
h.洗涤、干燥
(5)①根据各物质的溶解度曲线(见下图),在80℃时,用一定浓度的硫酸溶解“滤渣3”时,最适宜的硫酸浓度为_________。

A.3mol/L(1.20g/mL)
B.6mol/L(1.34g/mL)
C.9mol/L(1.49 g/mL)
D.18mol/L (1.84g/mL)
②所需硫酸用量的简便确定方法是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最活泼的金属元素、最活泼的非金属元素、常温下呈液态的金属(价电子排布为5d106s2)元素分别位于下面元素周期表中的( )

A. s区、p区、ds区 B. s区、p区、d区
C. f区、p区、ds区 D. s区、f区、ds区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com