
 ,
,
 ,E发生缩聚反应生成I为
,E发生缩聚反应生成I为 ,A和溴化氢发生加成反应生成B,则A中含有不饱和键,根据B的分子式可知,A的结构简式为:CH2=CHCH3,B为卤代烃,发生水解反应生成C,C中含有羟基,C发生氧化反应生成D,故B为CH3CH(Br)CH3,C为CH3CH(OH)CH3,据此解答.
,A和溴化氢发生加成反应生成B,则A中含有不饱和键,根据B的分子式可知,A的结构简式为:CH2=CHCH3,B为卤代烃,发生水解反应生成C,C中含有羟基,C发生氧化反应生成D,故B为CH3CH(Br)CH3,C为CH3CH(OH)CH3,据此解答. ,E发生缩聚反应生成I为
,E发生缩聚反应生成I为 ,A和溴化氢发生加成反应生成B,则A中含有不饱和键,根据B的分子式可知,A的结构简式为:CH2=CHCH3,B为卤代烃,发生水解反应生成C,C中含有羟基,C发生氧化反应生成D,故B为CH3CH(Br)CH3,C为CH3CH(OH)CH3,
,A和溴化氢发生加成反应生成B,则A中含有不饱和键,根据B的分子式可知,A的结构简式为:CH2=CHCH3,B为卤代烃,发生水解反应生成C,C中含有羟基,C发生氧化反应生成D,故B为CH3CH(Br)CH3,C为CH3CH(OH)CH3, ,故答案为:CH2=CHCH3;
,故答案为:CH2=CHCH3; ;
;| Cu/Ag |
| △ |
 +2H2O,
+2H2O,| H+ |
| △ |
| Cu/Ag |
| △ |
 +2H2O;CH3OH+CH2=C(CH3)COOH
+2H2O;CH3OH+CH2=C(CH3)COOH| H+ |
| △ |
 ,
, .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、碳酸钠(固体) |
| B、石灰水 |
| C、硫酸钾溶液 |
| D、硫酸铵(固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为; ③能与水在一定条件下反应生成C ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为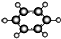 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为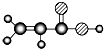 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B、将水加热,KW增大,pH不变 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D、向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
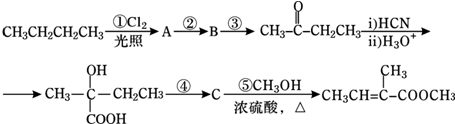
| H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | H+ | AsO33- | Sb3+ | Bi3+ | Fe2+ |
| c(mol?L-1) | 1.0 | 3.6×10-3 | 2.4×10-4 | 1.0×10-4 | 2.0×10-3 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com