
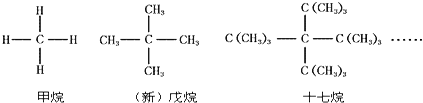
分析 (1)根据通式写出上一系列第4种烷烃的化学式;
(2)用数学中的数列通项求解的方法来解决,先将已知条件抽象为数学模型,观察分子式找出第n项分子式中氢原子数目为4×3(n-1),再根据烷烃通式求出碳原子数目,据此写出通式.
解答 解:(1)根据②的通式,将n=4代入,得碳原子数为2×3(4-1)-1=53,氢原子数目为4×3(4-1)=108,所以第4种烷烃的化学式为C53H108,
故答案为:C53H108;
②甲烷、新戊烷、十七烷分子中氢原子个数为等比数列:4、12、36…公比q=3,根据等比数列通项公式an=a1q(n-1),可知此烷烃的氢原子通项为4×3(n-1),设第n项的分子式为CmH2m+2,可得2m+2=4×3(n-1),解得m=2×3n-1-1,即该烷烃的碳原子通项为2×3n-1-1,所以该系列烷烃的化学式的通式为C2×3n-1-1H4×3n-1,
故答案为:C2×3n-1-1H4×3n-1(n≥1,且为正整数).
点评 本题考查了有机物分子式和结构式的确定,利用等比数列确定分子通式是解题关键,也是难点.


科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 还原性:HF<HCl<HBr<HI | B. | 稳定性:HF<HCl<HBr<HI | ||
| C. | 氧化性:F2<Cl2<Br2<I2 | D. | 沸点:Cl2<F2<Br2<I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ①③⑤ | C. | ②④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、Cu2+、NO3- | B. | Na+、Fe2+、H+、NO3- | ||
| C. | NH4+、Cl-、SO42-、OH- | D. | HCO3-、I-、Na+、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水鉴别苯、乙醇、四氯化碳 | |
| B. | 准确称取4.0 gNaOH溶于9 6 mL水得质量分数为4.0%的溶液 | |
| C. | 为除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤 | |
| D. | 用激光笔检验淀粉溶液的丁达尔现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com