
 ijæĪĶā»ī¶ÆŠ”×éÄ£Äā¹¤ŅµÖʱø“æ¼ī£¬·½°øČēĻĀ£ŗ
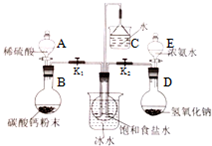
ijæĪĶā»ī¶ÆŠ”×éÄ£Äā¹¤ŅµÖʱø“æ¼ī£¬·½°øČēĻĀ£ŗ·ÖĪö Ķ¼ÖŠ×°ÖĆA”¢BÖĘČ”¶žŃõ»ÆĢ¼£¬×°ÖĆD”¢EÖĘČ”°±Ęų£¬°±Ęų¼«Ņ×ČÜÓŚĖ®£¬¶žŃõ»ÆĢ¼ŌŚĖ®ÖŠµÄČܽā¶Č½ĻŠ”£¬ĻČĶØČė°±Ęų£¬°±ĘųÓėĖ®ŠĪ³É³Ź¼īŠŌµÄ°±Ė®æÉÓė¶žŃõ»ÆĢ¼ÓėĖ®Éś³ÉµÄĢ¼Ėį·¢Éś·“Ó¦£¬øüÓŠĄūÓŚ¶žŃõ»ÆĢ¼ĘųĢåµÄĪüŹÕ£¬Ļņ±„ŗĶŹ³ŃĪĖ®ÖŠĶØČė×ćĮæ°±ĘųÖĮ±„ŗĶ£¬Č»ŗóĶØČė¶žŃõ»ÆĢ¼£¬Īö³öČܽā¶Č½ĻŠ”µÄĢ¼ĖįĒāÄĘ£¬Ģ¼ĖįĒāÄĘŹÜČČ·Ö½āÖʵĆĢ¼ĖįÄĘ£®
£Ø1£©ŹµŃéŠčŅŖÖʱøŌĮĻĘų°±ĘųÓė¶žŃõ»ÆĢ¼£¬×°ÖĆĘųĆÜŠŌŅŖŗĆ£»
£Ø2£©øł¾ŻŅĒĘ÷µÄ½į¹¹ĢŲÕ÷£¬æÉÖŖAĪŖ·ÖŅŗĀ©¶·£»ŃĪĖįŅ×»Ó·¢£¬ÓĆŃĪĖįÖĘČ”µÄ¶žŃõ»ÆĢ¼ÖŠ»ģÓŠĀČ»ÆĒā£¬ĀČ»ÆĒāÓėĢ¼ĖįÄĘ”¢Ģ¼ĖįĒāÄʶ¼ÄÜ·“Ó¦£»
£Ø3£©¶žŃõ»ÆĢ¼ŌŚĖ®ÖŠµÄČܽā¶Č½ĻŠ”£¬°±ĘųŅ×ČÜÓŚĖ®£¬ÖĘČ”Ģ¼ĖįĒāÄĘŹ±ĻČŅŖµĆµ½ŗ¬°±µÄ±„ŗĶŹ³ŃĪĖ®£»°±Ė®“ęŌŚĘ½ŗā£ŗNH3+H2O?NH3•H2O?NH4++OH-£¬øł¾ŻĘ½ŗāŅʶÆŌĄķ·ÖĪöÉś³É°±Ęų£»
“óŌ¼20·ÖÖÓ×óÓŅŹ±£¬¹Ū²ģµ½±„ŗĶŹ³ŃĪĖ®ÉĻ·½ÓŠÓŠ“óĮæµÄ°×ĪķŹ±£¬°±ĘųŌŚĀČ»ÆÄĘČÜŅŗÖŠŅŃ¾±„ŗĶ£»
£Ø4£©Ģ¼ĖįĒāÄĘ²»ĪČ¶Ø£¬ŌŚ¼ÓČČĢõ¼žĻĀÄÜ·Ö½āÉś³ÉĢ¼ĖįÄĘ”¢Ė®ŗĶ¶žŃõ»ÆĢ¼£¬ÅØĮņĖį¾ßÓŠĪüĖ®ŠŌ£¬ŌŁĶعż×ćĮæµÄ¹żŃõ»ÆÄĘ£¬·¢Éś·“Ó¦£ŗ2Na2O2+2CO2=2Na2CO3+O2£¬¹ĢĢåŌöÖŲĪŖÓė¶žŃõ»ÆĢ¼µČĪļÖŹµÄĮæµÄCOµÄÖŹĮ棬ŌŁøł¾Ż·½³ĢŹ½¼ĘĖć“æ¼īÖŹĮ森
½ā“š ½ā£ŗĶ¼ÖŠ×°ÖĆA”¢BÖĘČ”¶žŃõ»ÆĢ¼£¬×°ÖĆD”¢EÖĘČ”°±Ęų£¬°±Ęų¼«Ņ×ČÜÓŚĖ®£¬¶žŃõ»ÆĢ¼ŌŚĖ®ÖŠµÄČܽā¶Č½ĻŠ”£¬ĻČĶØČė°±Ęų£¬°±ĘųÓėĖ®ŠĪ³É³Ź¼īŠŌµÄ°±Ė®æÉÓė¶žŃõ»ÆĢ¼ÓėĖ®Éś³ÉµÄĢ¼Ėį·¢Éś·“Ó¦£¬øüÓŠĄūÓŚ¶žŃõ»ÆĢ¼ĘųĢåµÄĪüŹÕ£¬Ļņ±„ŗĶŹ³ŃĪĖ®ÖŠĶØČė×ćĮæ°±ĘųÖĮ±„ŗĶ£¬Č»ŗóĶØČė¶žŃõ»ÆĢ¼£¬Īö³öČܽā¶Č½ĻŠ”µÄĢ¼ĖįĒāÄĘ£¬Ģ¼ĖįĒāÄĘŹÜČČ·Ö½āÖʵĆĢ¼ĖįÄĘ£®
£Ø1£©Ä£Äā¹¤ŅµÖʱø“æ¼ī£ŗNaCl+H2O+NH3+CO2ØTNaHCO3”ż+NH4Cl£¬Ķ¼ÖŠ×°ÖĆA”¢BÖĘČ”¶žŃõ»ÆĢ¼£¬×°ÖĆD”¢EÖĘČ”°±Ęų£¬×°ÖĆĘųĆÜŠŌŅŖŗĆ£¬ĖłŅŌŅĒĘ÷°“ÉĻĶ¼×é×°ŗĆŗó£¬Ź×ĻČÓ¦øĆ½ųŠŠµÄ²Ł×÷ŹĒ¼ģŃé×°ÖĆĘųĆÜŠŌ£¬
¹Ź“š°øĪŖ£ŗ¼ģŃé×°ÖƵÄĘųĆÜŠŌ£»
£Ø2£©øł¾ŻŅĒĘ÷ĢŲµćæÉÖŖAĪŖ·ÖŅŗĀ©¶·£¬¶žŃõ»ÆĢ¼ĪŖÖʱø“æ¼īµÄŌĮĻĘųĢ壬ĀČ»ÆĒāÄÜŗĶĢ¼ĖįÄĘ”¢Ģ¼ĖįĒāÄĘ·“Ó¦£¬ĀČ»ÆĒāŅ×»Ó·¢£¬ÓĆŃĪĖįŗĶĢ¼ĖįøĘÖĘČ”µÄ¶žŃõ»ÆĢ¼ÖŠ»ģÓŠĀČ»ÆĒā£¬Ó°ĻģŗóŠų·“Ó¦£¬ĖłŅŌÓĆÄѻӷ¢µÄĮņĖį·Ö¶ą“ĪŗĶĢ¼ĖįøĘ·ŪÄ©·“Ó¦ÖĘČ”¶žŃõ»ÆĢ¼£¬
¹Ź“š°øĪŖ£ŗ·ÖŅŗĀ©¶·£»ŃĪĖįŅ×»Ó·¢£¬CO2ÖŠ»ģČėHCl£»
£Ø3£©Ņņ°±ĘųČܽā¶Č“ó£¬ĻČĶØČė°±ĘųŹ¹ČÜŅŗ³Ź¼īŠŌ£¬Ōö“ó¶žŃõ»ÆĢ¼µÄĪüŹÕĮ棬Ōö“óĢ¼ĖįĒāøłĄė×ÓµÄÅØ¶Č£¬ĖłŅŌŹµŃé¹ż³ĢÖŠĻČĶØČė°±Ęų£¬ĻČ“ņæŖK2£¬½«×°ÖĆEÖŠµÄŹŌ¼ĮĀżĀż¼ÓČėŌ²µ×ÉÕĘ棬ÉÕĘæÖŠĒāŃõ»ÆÄĘÓöĖ®·ÅČČ£¬Ķ¬Ź±µēĄė³ö“óĮæOH-Ąė×Ó£¬Ź¹NH3+H2O?NH3•H2O?NH4++OH-Ę½ŗāÄęĻņŅĘ¶Æ£¬²śÉś°±Ęų£¬“óŌ¼20·ÖÖÓ×óÓŅŹ±£¬¹Ū²ģµ½±„ŗĶŹ³ŃĪĖ®ÉĻ·½ÓŠ“óĮæµÄ°×ĪķŹ±£¬°±ĘųŌŚĀČ»ÆÄĘČÜŅŗÖŠŅŃ¾±„ŗĶ£¬ĖłŅŌŌŁ“ņæŖK1£¬ÖĘČ”¶žŃõ»ÆĢ¼ĶØČė¶žŃõ»ÆĢ¼·“Ó¦£¬
¹Ź“š°øĪŖ£ŗK2£»ĒāŃõ»ÆÄĘÓöĖ®·ÅČČ£¬Ķ¬Ź±µēĄė³ö“óĮæOH-Ąė×Ó£¬Ź¹NH3+H2O?NH3•H2O?NH4++OH-Ę½ŗāÄęĻņŅĘ¶Æ£¬²śÉś°±Ęų£»“óĮæµÄ°×Īķ£»K1£»
£Ø4£©Ģ¼ĖįĒāÄĘŹÜČČ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ2NaHCO3$\frac{\underline{\;\;”÷\;\;}}{\;}$Na2CO3+CO2”ü+H2O£¬ÅØĮņĖį¾ßÓŠĪüĖ®ŠŌ£¬ŌŁĶعż×ćĮæµÄ¹żŃõ»ÆÄĘ£¬2Na2O2+2CO2=2Na2CO3+O2£¬¹ĢĢåŌöÖŲĪŖÓė¶žŃõ»ÆĢ¼µČĪļÖŹµÄĮæµÄCOµÄÖŹĮ棬n£ØCO£©ØT0.1mol£¬øł¾ŻĢ¼Ō×ÓŹŲŗć£ŗn£ØCO2£©=n£ØCO£©=$\frac{0.28g}{28g/mol}$0.01mol£¬
ÓÉ2NaHCO3$\frac{\underline{\;\;”÷\;\;}}{\;}$Na2CO3+CO2”ü+H2O£¬æÉÖŖn£ØNa2CO3£©=n£ØCO2£©=0.01mol£¬ŌņÖʵƵēæ¼īÖŹĮæĪŖ£ŗm£ØNa2CO3£©=nM=0.01mol”Į106g/mol=1.06g£¬
¹Ź“š°øĪŖ£ŗ¼ÓČČ£Ø»ņ×ĘÉÕ£©£»2NaHCO3$\frac{\underline{\;\;”÷\;\;}}{\;}$Na2CO3+H2O+CO2”ü£»1.06£®
µćĘĄ ±¾ĢāŹĒŅ»µĄÓŠ¹Ų¹¤ŅµÖĘ“æ¼īÖŖŹ¶µÄ×ŪŗĻŹµŃéĢāÄ棬漲éѧɜ·ÖĪöŗĶ½ā¾öĪŹĢāµÄÄÜĮ¦£¬ÕĘĪÕÖĘ¼īŌĄķŹĒ½āĢāµÄ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 æŚĖćĢāĢģĢģĮ·ĻµĮŠ“š°ø
æŚĖćĢāĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹čŹĒÖĘŌģĢ«ŃōÄܵē³ŲµÄ³£ÓĆ²ÄĮĻ | |
| B£® | ĖÄŃõ»ÆČżĢśĖ׳ĘĢśŗģ£¬æÉÓĆÓŚ×÷ÓĶĘį”¢ŗģÉ«ĶæĮĻ | |
| C£® | Na2O2æÉÓĆ×÷ŗōĪüĆę¾ßÖŠµÄ¹©Ńõ¼Į | |
| D£® | ¶žŃõ»Æ¹čŹĒÖĘŌģ¹āµ¼ĻĖĪ¬µÄ²ÄĮĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü | B£® | ¢Ū¢Ü | C£® | ¢Ś¢Ū¢Ü | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪļĄķŠŌÖŹ | ÖʱøŌĄķ | »ÆѧŠŌÖŹ |
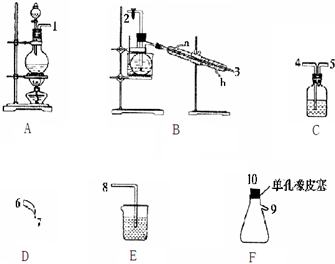
| »ĘÉ«ÓĶדŅŗĢå ČŪµćĪŖ-40”ę£¬·ŠµćĪŖ71”ę ²»ČÜÓŚĄäĖ®£¬Ņ×ČÜÓŚÓŠ»śČܼĮ ĆܶČĪŖ1.65g/mL | Cl2ÓėNH4ClĖ®ČÜŅŗŌŚµĶĪĀĻĀ·“Ó¦ | 95”걬ÕØ£¬ČČĖ®ÖŠ·¢ÉśĖ®½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘųČÜÓŚĖ®£ŗCl2+H2OØT2H++Cl-+ClO- | |
| B£® | ĻņNa2SiO3ČÜŅŗÖŠĶØČėÉŁĮæCO2£ŗSiO32-+CO2+H2OØTH2SiO3”ż+CO32- | |
| C£® | ĀĮ·ŪĶ¶ČėNaOHČÜŅŗÖŠ£ŗ2Al+2OH-ØT2AlO2-+H2”ü | |
| D£® | AlCl3ČÜŅŗÖŠ¼ÓČė×ćĮæ°±Ė®£ŗAl3++3OH-ØTAl£ØOH£©3”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
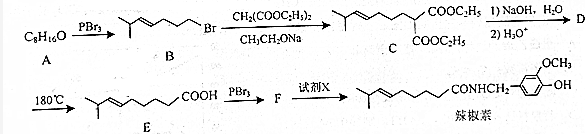
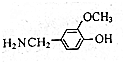 £¬ÓÉB”śCµÄ·“Ó¦ĄąŠĶŹĒČ”“ś£¬
£¬ÓÉB”śCµÄ·“Ó¦ĄąŠĶŹĒČ”“ś£¬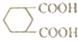 µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£¬ÉĻŹöĮ÷³ĢÖŠ³öĻֵďŌ¼ĮæÉÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗCH2=CH2$\stackrel{HBr}{”ś}$^CH3CH2Br$”ś_{”÷}^{NaOHČÜŅŗ}$CH3CH2OH£®
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£¬ÉĻŹöĮ÷³ĢÖŠ³öĻֵďŌ¼ĮæÉÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗCH2=CH2$\stackrel{HBr}{”ś}$^CH3CH2Br$”ś_{”÷}^{NaOHČÜŅŗ}$CH3CH2OH£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
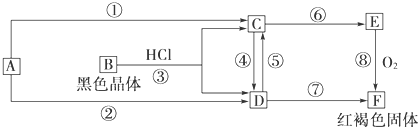
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²»·“Ó¦ | B£® | ÉÕ±ÄŚČÜŅŗŃÕÉ«Öš½„±äŗģ | ||
| C£® | ½šŹōÄĘ³ĮČėÉÕ±µ×²æ£¬²¢²śÉśĘųÅŻ | D£® | ½šŹōÄĘø”ÓŚŅŗĆęÉĻ£¬ĖÄ“¦ÓĪ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®Äą | B£® | ²£Į§ | C£® | ŹÆ»ŅŹÆ | D£® | ĢÕ“É |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com