
提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是( )
| 选项 | 不纯物质 | 除杂试剂 | 分离方法 |
| A | 苯(甲苯) | 酸性高锰酸钾溶液 | 分液 |
| B | 氯化铵溶液(氯化铁) | 氢氧化钠溶液 | 过滤 |
| C | 乙酸乙酯(乙酸) | 氢氧化钾溶液 | 分液 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是( )
A.醋酸钠的水解反应CH3COO-+H3O+===CH3COOH+H2O
B.碳酸氢钙与少量的NaOH溶液反应Ca2++2HCO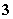 +2OH-===CaCO3↓+2H2O+CO
+2OH-===CaCO3↓+2H2O+CO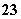
C.向AgCl悬浊液中滴加NaI溶液AgCl(s)+I-(aq)===AgI(s)+Cl-(aq)
D.稀硝酸与过量的铁屑反应Fe+4H++NO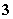 ===Fe3++NO↑+2H2O
===Fe3++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关σ键的说法错误的是( )
A.如果电子云图象是由两个s电子重叠形成的,即形成ss σ键
B.s电子与p电子可形成sp σ键
C.p电子与p电子不能形成σ键
D.HCl分子里含一个sp σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是A、B、C、D、E五种元素的某些性质:
|
| A | B | C | D | E |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是________。
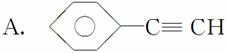
B.CH4
C.CH2===CHCH3
D.CH3CH2C≡CH
E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键___________________________________________。
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是________(化学式),理由是________________________。
(4)B、D形成的氢化物沸点:________更高,热稳定性________更强。(写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
含有氨基(—NH2)的化合物通常能够与盐酸反应,生成盐酸盐,如:
R—NH2+HCl—→R—NH2·HCl(R—代表烷基、苯基等)
现有两种化合物A和B,它们互为同分异构体。已知:
①它们都是对位二取代苯;②它们的相对分子质量都是137;③A既能被NaOH溶液中和,又可以跟盐酸成盐,但不能与FeCl3溶液发生显色反应;B既不能被NaOH溶液中和,也不能跟盐酸成盐;④它们的组成元素只可能是C、H、O、N、Cl中的几种。
请按要求填空:
(1)A和B的分子式是________。
(2)A的结构简式是________;B的结构简式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
B. 1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA
C.8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA
D.t℃时,MgCO3的KSP=4×10-6,,则饱和溶液中含Mg2+数目为2×10-3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
1.6 g NaOH恰好与20 mL的盐酸完全反应,则盐酸的物质的量浓度为( )
A.0.2 mol·L-1 B.2 mol·L-1
C.0.5 mol·L-1 D.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素。已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个单电子,G的核电荷数比F多5。请回答下列问题(用相应的元素符号、化学式和化学术语填空)
(1)G在周期表中的位置是____,F元素的原子基态价层电子排布式__ 。
(2)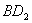 分子的电子式为__________,
分子的电子式为__________,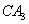 分子的空间立体构型为__________。
分子的空间立体构型为__________。
(3)A元素分别与B、D元素形成的两种微粒H、I都具有N2H4相似的结构,属于等电子数微粒,它们的化学式分别是H:__________、I:__________。
(4)向G的硫酸盐溶液中逐滴加入足量的氨水至得到的沉淀完全溶解,再向该溶液中加入一定量乙醇,析出一种深蓝色晶体。在该晶体中存在的化学键的种类有__________。
 (5)0.3g H在足量氧气中燃烧,生成气态
(5)0.3g H在足量氧气中燃烧,生成气态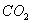 和液态
和液态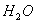 ,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。
,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。
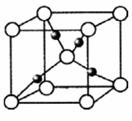
(6)G的一种氧化物的晶胞结构如图所示(黑球代表G原子),该氧化物的化学式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com