
| A. | C7H16主链上有5个碳原子的同分异构体有5种 | |
| B. | 按系统命名法,化合物的名称是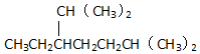 2,6-二甲基-3-乙基庚烷 2,6-二甲基-3-乙基庚烷 | |
| C. | 乙炔分子的球棍模型: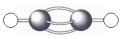 | |
| D. | 卤代烃加入硝酸酸化的硝酸银溶液根据生成的卤化银沉淀颜色检验卤原子 |
分析 A.烷烃的同分异构体只存在碳链异构,根据定位法确定分子式为C7H16,主链上为五个碳原子的有机物的种数即可;
B.烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上的碳原子进行编号;
C.球棍模型表示原子间的连接与空间结构;
D.卤代烃不能电离出卤素离子.
解答 解:A.C7H16为庚烷,主链上有5个碳原子的同分异构体有:2,3-二甲基戊烷,2,4-二甲基戊烷,2,2-二甲基戊烷,3,3-二甲基戊烷,3-乙基戊烷,共5种,故A正确;
B.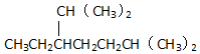 最长的碳链有7个碳原子,该有机物名称为:2,6-二甲基-3-乙基庚烷,故B正确;
最长的碳链有7个碳原子,该有机物名称为:2,6-二甲基-3-乙基庚烷,故B正确;
C.乙炔中存在碳碳三键,分子的球棍模型: ,故C正确;
,故C正确;
D.卤代烃为非电解质,不能电离出卤素离子,应先在碱性条件下水解,故D错误.
故选D.
点评 本题考查有机物的结构与性质,把握官能团与性质的关系、有机反应及有机物检验等为解答的关键,综合性较强,注重基础知识的考查,题目难度不大.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:选择题
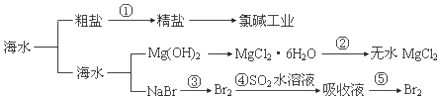
| A. | 粗盐可采用除杂和重结晶等过程提纯 | |
| B. | 工业生产中常选用石灰乳作为 Mg2+的沉淀剂 | |
| C. | 第②步的反应条件是:在空气中直接加热 | |
| D. | 第③步到第⑤步的目的是为了富集溴元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  图是除去水中泥沙 | B. |  图是配制0.100 mol/L稀硫酸 | ||
| C. |  图是点燃酒精灯 | D. |  图是检查装置的气密性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
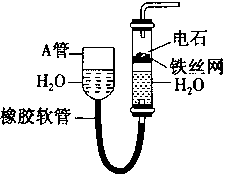 如图中的实验装置可用于制取乙炔.请填空:
如图中的实验装置可用于制取乙炔.请填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
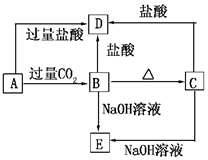 A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃).
A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
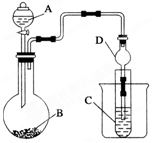 为探究元素的非金属性的变化规律,某化学兴趣小组同学设计了如下一系列实验,利用如图所示装置:
为探究元素的非金属性的变化规律,某化学兴趣小组同学设计了如下一系列实验,利用如图所示装置:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
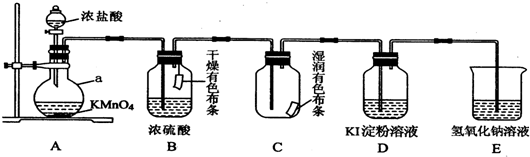
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com