



科目:高中化学 来源: 题型:
A、F结构示意图为: | ||||
B、HCl的电子式为:H+[:
| ||||
C、Na2O2的形成过程可以表示为: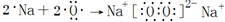 | ||||
| D、次氯酸(HClO)的结构式为:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(NH4+ )相等的NH4HSO4 和NH4Cl 溶液中,溶质浓度大小关系:c(NH4HSO4)<c(NH4Cl) |
| B、向10mL 0.10CH3COOH溶液中加入一定量的NaOH后,溶液成中性;c(Na+ )=c(CH3COO-)>c(OH-)=c(H+) |
| C、两种不同浓度的HA溶液的物质量浓度分别为c1和c2,pH 分别为a和(a+1),则有c1≤10c2 |
| D、NaHCO3溶液中,c(H+)+c(H2CO3)=c(CO3 2-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、炒菜的铁锅容易生锈 |
| B、盛放氯气的钢瓶久置后表面变暗 |
| C、运输石油的管道表面变暗 |
| D、银质奖牌(纯银制成)久置后表面变暗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、23gNa中,原子总数为NA |
| B、2L浓度为1mol/L NaCl溶液中,Na+的总数为2NA |
| C、16g O2所含的分子数为NA |
| D、标况下11.2L 的CH4,分子总数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | HA物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 装置可用于分离I2与NH4Cl混合物 |
B、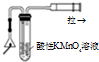 装置可用于检验火柴头燃烧产生的SO2 |
C、 装置可用乙醇萃取碘水中的碘 |
D、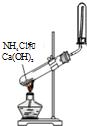 装置可用于实验室制取和收集少量氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com