
| t/℃ | 700 | 800 | 850 | 1000 | 1200 |
| K1 | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

| 起始浓度 | 甲 | 乙 | 丙 |
| c(CO2)(mol/L) | 0.01 | 0.02 | 0.02 |
| c(H2)(mol/L) | 0.01 | 0.01 | 0.02 |
| 0.20mol/L-0.08mol/L |
| 4min |
| 0.18×0.08 |
| 0.12×0.12 |
| x2 |
| (0.02-x)2 |
| 0.02-0.008 |
| 0.02 |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2012-2013学年江西省赣州市十一县(市)高一上学期期中联考化学试卷(带解析) 题型:填空题
已知下列两个反应①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓)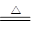 CuSO4+SO2↑+2H2O。试回答下列问题:
CuSO4+SO2↑+2H2O。试回答下列问题:
(1)反应①中 元素被还原,反应②中 元素被还原.
(2)当反应①生成2gH2时,消耗H2SO4的物质的量是 。
(3)反应②若有1mol H2SO4作氧化剂时,转移电子的物质的量为 ,若有4mol H2SO4参加反应时,被还原元素的质量是 g。
查看答案和解析>>
科目:高中化学 来源:2013届天津市天津一中高三第四次月考化学试卷(带解析) 题型:推断题
物质A为生活中常见的有机物,只含有C、H、O三种元素,且它们的质量比为12∶3∶8。物质D是一种芳香族化合物,请根据如图(所有无机产物已略去)中各有机物的转化关系回答问题。
已知,两分子醛在一定条件下可以发生如下反应(其中R、R′为H或烃基):
(1) 写出物质A的结构简式: ____;C的名称: ______;E中含氧官能团的名称:_______。
(2) 写出下列反应的有机反应类型:A→B____________________; E→F____________________
(3) 写出H与G反应生成I的化学方程式: ___________________________________________。
(4) 写出D与新制氢氧化铜反应的化学方程式:
____________________________________________________________________。
(5) 若F与NaOH溶液发生反应,则1 mol F最多消耗NaOH的物质的量为_____mol。
(6) E有多种同分异构体,与E具有相同官能团的芳香族同分异构体有________种(包括本身和顺反异构),写出其中核磁共振氢谱有五个吸收峰的同分异构体的结构简式:
____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省常州市高二上学期期中考试化学试卷(解析版) 题型:填空题
(1)有机物A由C、H、O三种元素组成,其蒸气密度是同温同压下氢气密度的23倍,核磁共振氢谱显示其分子中有3种氢原子且个数比为3:2:1 。有机物A的分子式为 。
(2)芳香化合物B的分子式为C7H8O,B能与金属钠反应,不与强碱反应。B中所含官能团的名称 ;B的同分异构体中能与FeCl3溶液发生显色反应的物质有多种,请任写一种结构简式 。
(3)用A和B为原料完成以下转化:

已知:①两个醛分子间能发生如下反应:
 (﹣R、﹣R’表示氢原子或烃基)
(﹣R、﹣R’表示氢原子或烃基)

③1mol H分别与足量的金属钠、碳酸氢钠溶液反应时,均生成22.4L气体(标准状况)。
回答下列问题:
① C + D E的反应类型为 ;E
E的反应类型为 ;E F反应的反应类型为____________。
F反应的反应类型为____________。
②F的结构简式为: 。
③写出下列转化的化学方程式:
B D
。
D
。
D K
。
K
。
H I
。
I
。
④满足下列条件的F有多种同分异构体,
Ⅰ. 该物质和FeCl3溶液能发生显色反应;
Ⅱ.该物质能使Br2的CC14溶液褪色;
Ⅲ.该物质分子中只有一个甲基。
写出其中苯环上取代基数目不同的任意两种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市高三毕业班联考(一)理综化学试卷(解析版) 题型:填空题
(1)有机物A由C、H、O三种元素组成,其蒸气密度是同温同压下氢气密度的23倍,核磁共振氢谱显示其分子中有3种氢原子且个数比为3:2:1 。有机物A的分子式为 。
(2)芳香化合物B的分子式为C7H8O,B能与金属钠反应,不与强碱反应。B中所含官能团的名称 ;B的同分异构体中能与FeCl3溶液发生显色反应的物质有多种,请任写一种结构简式 。
(3)用A和B为原料完成以下转化:
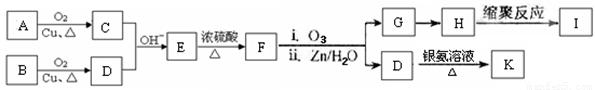
已知:①两个醛分子间能发生如下反应:
 (﹣R、﹣R’表示氢原子或烃基)
(﹣R、﹣R’表示氢原子或烃基)

③1mol H分别与足量的金属钠、碳酸氢钠溶液反应时,均生成22.4L气体(标准状况)。
回答下列问题:
① C + D E的反应类型为
;E
E的反应类型为
;E F反应的反应类型为____________。
F反应的反应类型为____________。
②F的结构简式为: 。
③写出下列转化的化学方程式:
B D
。
D
。
D K
。
K
。
H I
。
I
。
④满足下列条件的F有多种同分异构体,
Ⅰ. 该物质和FeCl3溶液能发生显色反应;
Ⅱ.该物质能使Br2的CC14溶液褪色;
Ⅲ.该物质分子中只有一个甲基。
写出其中苯环上取代基数目不同的任意两种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2015届江西省赣州市十一县(市)高一上学期期中联考化学试卷(解析版) 题型:填空题
已知下列两个反应①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓)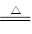 CuSO4+SO2↑+2H2O。试回答下列问题:
CuSO4+SO2↑+2H2O。试回答下列问题:
(1)反应①中 元素被还原,反应②中 元素被还原.
(2)当反应①生成2gH2时,消耗H2SO4的物质的量是 。
(3)反应②若有1mol H2SO4作氧化剂时,转移电子的物质的量为 ,若有4mol H2SO4参加反应时,被还原元素的质量是 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com