
【题目】Calanolide A是一种抗HIV药物,其结构简式如下图所示。已知:碳原子上连有4个不同的原子或基团时,该碳称为手性碳。下列关于Calanolide A的说法不正确的是( )
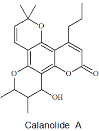
A.分子中有3个手性碳原子
B.分子中有5种含氧官能团
C.能发生消去反应、加成反应、氧化反应和还原反应
D.1molCalanolide A最多消耗2molNaOH或5molH2
【答案】B
【解析】
A.根据手性碳原子的定义,该物质中有3个手性碳原子,将用“*”标识,如图所示,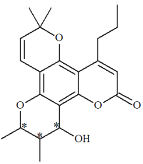 ,A正确,不选;
,A正确,不选;
B.分子中含有3种含氧官能团,分别为羟基、醚键、酯基,B错误,符合题意;
C.分子中含有羟基,且与其相连的碳原子有相邻的碳原子且与此相邻的碳原子上连有氢原子,可以发生消去反应;含有苯环、碳碳双键,可以与氢气发生加成反应,也是还原反应;碳碳双键、羟基等可以被氧化,可以发生氧化反应,C正确,不选;
D.分子中含有酯基,该酯基在酸性条件下水解后得到羧基和与苯环相连的羟基,均可与NaOH反应,则1molCalanolide A最多消耗2molNaOH;1mol苯环可与3molH2加成,1mol碳碳双键可与1molH2加成,1molCalanolide A含有1mol苯环和2mol碳碳双键,可与5molH2发生加成,D正确,不选;
答案选B。


科目:高中化学 来源: 题型:
【题目】天然气水蒸汽重整法是工业上生产氢气的重要方法,反应在 400℃以上进行。l 00kPa 时,在反应容器中通入甲烷与为水蒸汽体积比为1 : 5的混合气体,发生下表反应。
反应方程式 | 焓变△H(kJ/mol) | 600℃时的平衡常数 |
①CH4(g)+ H2O(g) | a | 0.6 |
②CH4(g)+ 2H2O(g) | +165.0 | b |
③CO(g)+ H2O(g) | -41.2 | 2.2 |
请回答下列下列问题:
(1)上表中数据 a=__________; b= ___________ 。
(2)对于反应②,既能加快反应又能提高CH4转化率的措施是_____________。
A.升温 B.加催化剂 C.加压 D.吸收CO2
(3)下列情况能说明容器中各反应均达到平衡的是___________。
A.体系中H2O与CH4物质的量之比不再变化
B.体系中H2的体积分数保持不变
C.生成n 个CO2的同时消耗2n个H2O
D. v正(CO)= v逆(H2)
(4)工业重整制氢中,因副反应产生碳会影响催化效率,需要避免温度过高以减少积碳。该体系中产生碳的反应方程式为 _______________。
(5)平衡时升温,CO含量将_________(选填“增大”或“减小”)。
(6)一定温度下 ,平衡时测得体系中 CO2和H2的物质的量浓度分别是0.75mo l/L、4.80mol/L , 则此时体系中CO 物质的量浓度是_______ mol/L。
(7)改变上述平衡体系的温度,平衡时H2O与CH4物质的量之比[![]() ]值也会随着改变,在图中画出其变化趋势。________________
]值也会随着改变,在图中画出其变化趋势。________________
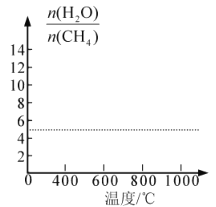
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,H2和O2在Ag9(图中物质1)团簇上生成H2O2的吉布斯自由能(![]() )的部分变化曲线如图。下列说法错误的是( )
)的部分变化曲线如图。下列说法错误的是( )
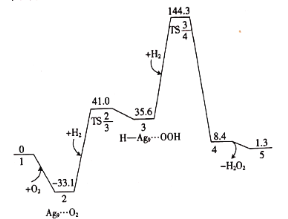
A.物质2中的O2是处于被吸附活化状态
B.物质3→物质4的过程中活化吉布斯自由能能垒为![]()
C.物质4可能为![]()
D.反应![]() 具有自发性
具有自发性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸H2A为二元弱酸.20℃时,配制一组c(H2A)+c(HA﹣)+c(A2﹣)=0.100molL﹣1的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
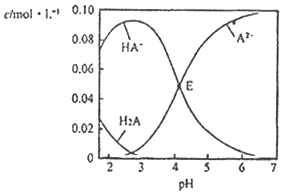
A.pH=2.5的溶液中:c(H2A)+c(A2﹣)>c(HA﹣)
B.c(Na+)=0.100moLL﹣1的溶液中:c(H+)+c(H2A)=c(OH﹣)+c(A2﹣)
C.c(HA﹣)=c(A2﹣)的溶液中:c(Na+)>0.100molL﹣1+c(HA﹣)
D.pH=7.0的溶液中:c(Na+)<2c(A2﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)碳酸:H2CO3,K1=4.3×10﹣7,K2=5.6×10﹣11
草酸:H2C2O4,K1=5.9×10﹣2,K2=6.4×10﹣5
0.1mol/L Na2CO3溶液的pH_____0.1mol/L Na2C2O4溶液的pH;(选填“大于”“小于”或“等于”)
(2)等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是_____;若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____(选填编号);
a.c(H+)>c(HC2O![]() )>c(HCO
)>c(HCO![]() )>c(CO
)>c(CO![]() )
)
b.c(HCO![]() )>c(HC2O
)>c(HC2O![]() )>c(C2O
)>c(C2O![]() )>c(CO
)>c(CO![]() )
)
c.c(H+)>c(HC2O![]() )>c(C2O
)>c(C2O![]() )>c(CO
)>c(CO![]() )
)
d.c(H2CO3)>c(HCO![]() )>c(HC2O
)>c(HC2O![]() )>c(CO
)>c(CO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用的食品抗氧化剂BHT的合成方法如下图所示(假设原料均能恰好完全反应):

下列说法中不正确的是( )
A.方法一的原子利用率为100%
B.方法二属于取代反应
C.X与Y均能与![]() 、
、![]() 溶液、溴水发生反应
溶液、溴水发生反应
D.![]() 在稀
在稀![]() 条件下发生消去反应可生成
条件下发生消去反应可生成![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成单质和化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图所示:
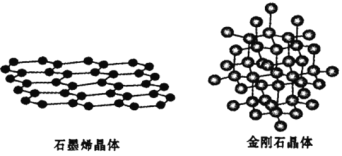
石墨烯能导电而金刚石不能导电的原因是________。
(2)碳的主要氧化物有CO和CO2
①CO能与金属Fe形成一种浅黄色液体Fe(CO)5,其熔点为-20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:该化合物的晶体中不涉及的作用力有________。
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②CO2在一定条件下可以合成甲醇,反应方程式为:![]() 。该反应所涉及的4种物质,沸点从高到低的顺序为________。
。该反应所涉及的4种物质,沸点从高到低的顺序为________。
(3)![]() 是重要的有机反应中间体,其空间构型为________。
是重要的有机反应中间体,其空间构型为________。
(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图所示。
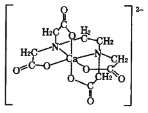
①钙离子的配位数是________。
②配体中碳原子的杂化方式有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏伽德罗常数的数值,下列叙述正确的是( )
A.![]() 与
与![]() 混合物中含
混合物中含![]() 原子数为NA
原子数为NA
B.![]() 正丁烷和
正丁烷和![]() 异丁烷的混合物中共价键数目为1.4NA
异丁烷的混合物中共价键数目为1.4NA
C.![]() 、
、![]() 时,
时,![]() 完全燃烧消耗
完全燃烧消耗![]() 分子数为0.15NA
分子数为0.15NA
D.![]() 甲烷与足量氯气在光照下充分反应后产物中含有的
甲烷与足量氯气在光照下充分反应后产物中含有的![]() 分子数为NA
分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
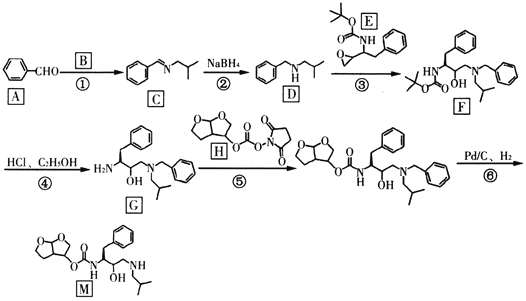
【题目】“达芦那韦”是抗击新型冠状病毒潜在用药,化合物M是它的合成中间体,其合成路线如下:
已知:R1CHO![]()
![]()
回答下列问题:
(1)有机物A的名称是______________;反应②反应类型是__________。
(2)物质B的结构简式是____________;E的分子式为_____________。
(3)G中含氧官能团的名称是________;F中有________个手性碳原子。
(4)请写出反应⑤的化学反应方程式_____________。
(5)物质N是C的一种同分异构体,写出满足下列条件的一种同分异构体的结构简式_______。
①分子结构中含有苯环和氨基,氨基与苯环直接相连;②能使溴水褪色;③核磁共振氢谱有6组峰,峰面积之比为6∶3∶2∶2∶1∶1。
(6)设计由苯甲醇和CH3NH2为原料制备![]() 的合成路线_______________。
的合成路线_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com