
【题目】【化学——选修5:有机化学基础】目前,回收溴单质的方法主要有水蒸气蒸馏法和萃取法等.某兴趣小组通过查阅相关资料拟采用如下方案从富马酸废液(含溴0.27%)中回收易挥发的Br2:
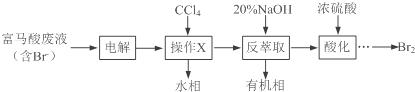
(1)操作X所需要的主要玻璃仪器为____________;反萃取时加入20%的NaOH溶液,其离子方程式为________________________.
(2)反萃取所得水相酸化时,需缓慢加入浓硫酸,并采用冰水浴冷却的原因是_________.
(3)溴的传统生产流程为先采用氯气氧化,再用空气水蒸气将Br2吹出.与传统工艺相比,萃取法的优点是____________________________.
(4)我国废水三级排放标准规定:废水中苯酚的含量不得超过1.00mg/L.实验室可用一定浓度的溴水测定某废水中苯酚的含量,其原理如下:
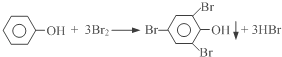
①请完成相应的实验步骤:
步骤1:准确量取25.00mL待测废水于250mL锥形瓶中.
步骤2:将4.5mL 0.02mol/L溴水迅速加入到锥形瓶中,塞紧瓶塞,振荡.
步骤3:打开瓶塞,向锥形瓶中加入过量的0.1mol/L KI溶液,振荡.
步骤4:____________________________,再用0.01mol/L Na2S2O3标准溶液滴定至终点,消耗 Na2S2O3溶液15mL.(反应原理:I2+2Na2S2O3=2NaI+Na2S4O6)
步骤5:将实验步骤1~4重复2次.
②该废水中苯酚的含量为____________mg/L.
③步骤3若持续时间较长,则测得的废水中苯酚的含量_________________(填“偏高”、“偏低”或“无影响”).
【答案】分液漏斗Br2+2OH﹣=Br﹣+BrO﹣+H2O减少Br2的挥发没有采用有毒气体Cl2,更环保滴入2~3滴淀粉溶液18.8mg/L偏低.
【解析】
富马酸废液中含有Br-,电解生成溴单质,加入四氯化碳萃取后分液,再加入氢氧化钠反萃取得到含修炼者和次溴酸根离子的溶液,加入硫酸酸化发生氧化还原反应生成溴单质;
(1)操作X为萃取分液,需要烧杯、分液漏斗等仪器;反萃取时加入20%的NaOH溶液反应生成溴化钠、次溴酸钠和水,反应的离子方程式为:Br2+2OH-=Br-+BrO-+H2O;
(2)溴单质易挥发,浓硫酸溶解放热分析,反萃取所得水相酸化时,需缓慢加入浓硫酸,并采用冰水浴冷却的原因是减少溴单质的挥发;
(3)无有毒气体氯气参加反应,生产过程环保;
(4)①硫代硫酸钠溶液滴定碘单质,加入淀粉溶液做指示剂;滴入2~3滴淀粉溶液,再用0.01mol/LNa2S2O3标准溶液滴定至终点;
②依据化学方程式定量关系计算,将4.5mL0.02mol/L溴水迅速加入到锥形瓶中,n(Br2)=0.0045L×0.02mol/L=0.00009mol,其中和碘化钾反应的溴单质物质的量
2KI~Br2~I2~2Na2S2O3,;
1 2
n0.01mol/L×0.015L
n=0.000075mol
与苯酚反应的溴单质=0.00009mol-0.000075mol=0.000015mol
则苯酚物质的量=![]() ×0.000015mol=0.000005mol
×0.000015mol=0.000005mol
该废水中苯酚的含量为=![]() ×0.000005mol×94g/mol=0.0188g/L=18.8mg/L;
×0.000005mol×94g/mol=0.0188g/L=18.8mg/L;
③步骤3持续的时间长导致的是KI被氧化,测定苯酚量减少,测定结果偏低。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】假设反应N2+3H22NH3(正反应为放热反应) 的正反应速率是v1 , 逆反应速率是v2 , 当升高温度时,v1和v2的变化情况为( )
A.同时增大
B.v1减小,v2增大
C.同时减小
D.v1增大,v2减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃时,下列反应的平衡常数如下:
①N2(g)+O2(g)![]() 2NO(g) K1=1×10-30
2NO(g) K1=1×10-30
②2H2(g)+O2(g)![]() 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
③2CO2(g)![]() 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92
下列说法正确的是
A.NO分解反应NO(g)![]()
![]() N2(g)+
N2(g)+![]() O2(g)的平衡常数为1×10-30
O2(g)的平衡常数为1×10-30
B.根据K2的值可以判断常温下H2和O2很容易反应生成H2O
C.常温下,NO、H2O、CO2三种物质分解放出O2的倾向顺序为NO>H2O>CO2
D.温度升高,上述三个反应的平衡常数均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中,能使电离平衡的是H2O![]() H++OH-向右移动且溶液呈酸性的是( )
H++OH-向右移动且溶液呈酸性的是( )
A. 向水中加入NaHSO4溶液 B. 向水中加入Al2(SO4)3固体
C. 向水中加入Na2CO3溶液 D. 将水加热到100℃,使pH=6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,右向所得硝酸铜溶液中加入5mol·L-1 NaOH溶液至Cu2+恰好完全沉淀, 则消耗 NaOH溶液的体积是
A. 15mL B. 30 mL C. 45 mL D. 60 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义
(1)硫酸生产过程中2SO2(g)+O2(g)2SO3(g),平衡混合体系中 SO3的百分含量和温度的关系如图1所示,根据图1回答下列问题:
①2SO2(g)+O2(g)2SO3(g)的△H____0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是____.
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化
d.单位时间内转移4mol 电子,同时消耗2mol SO3
e.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g)2NH3(g).图2表示在此反应过程中的能量的变化,图3表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图4表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.
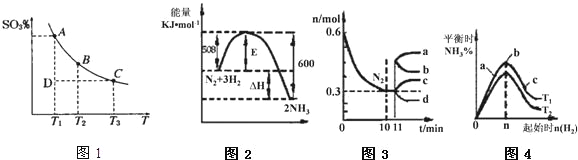
①该反应的平衡常数表达式为_____,升高温度,平衡常数______(填“增大”或“减小”或“不变”).
②由图2信息,计算0~10min内该反应的平均速率v(H2)=______,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为______(填“a”或“b”或“c”或“d”).
③图3a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是______点,温度T1______T2(填“>”或“=”或“<”).
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈_____性,所得溶液中c(H+)﹣c(OH﹣)=_________________(填写表达式)(已知:H2SO3:Ka1=1.7×10﹣2,Ka2=6.0×10﹣8,NH3H2O:Kb=1.8×10﹣5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是重要的工业原料。
(1)标准状况下,将500L氨气溶与水形成1L氨水,则此氨水的物质的量浓度为______mol/L(保留三位有效数字),该氨水最多能吸收二氧化硫的体积为_________。
(2)氨的催化氧化是重要的工业生产,此反应将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为__________________。下列反应中的氨与氨催化氧化中的氨性质相同的是________________。
A.2Na+2NH3=2NaNH2+H2↑
B.2NH3+3CuO=3Cu+N2+3H2O
C.4NH3+6NO=5N2+6H2O
D.HNO3+NH3=NH4NO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:则下列说法正确的是
①CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1

A. H2的燃烧热为241.8kJ·mol-1
B. 由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol-1
C. H2(g)转变成H2O(g)的化学反应一定要释放能量
D. 根据②推知反应H2(g) +1/2O2(g)=H2O(l):ΔH>-241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质性质的说法正确的是( )
A.通常状况下,NO2是无色的气体
B.SO2能漂白品红等物质,说明SO2有氧化性
C.氯化钙溶液和AgNO3溶液混合有白色沉淀产生
D.加热时,铁单质与浓硝酸不发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com