
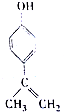
| A. | 该物质的分子式是C9H11O | |
| B. | 该物质分子中的所有C原子可以共面 | |
| C. | 滴入KMnO4(H+)溶液,可观察到紫色褪去,能证明结构中存在碳碳双键 | |
| D. | 1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别是3mol、4mol |
分析 A.根据结构简式确定分子式;
B.根据乙烯和苯的结构判断该分子中C原子是否共面,乙烯和苯是平面结构,乙烯和苯分子中所有原子都共面;
C.碳碳双键、酚羟基都能被酸性高锰酸钾溶液氧化;
D.苯环上酚羟基邻位氢原子能和溴发生取代反应,碳碳双键和溴发生加成反应,苯环和碳碳双键能和氢气在一定条件下发生加成反应.
解答 解:A.根据结构简式确定分子式为C9H10O,故A错误;
B.乙烯和苯是平面结构,乙烯和苯分子中所有原子都共面,根据乙烯和苯的结构知,该分子中所有碳原子可以共面,故B正确;
C.碳碳双键、酚羟基都能被酸性高锰酸钾溶液氧化,所以不能根据是否使酸性高锰酸钾溶液褪色来确定是否含有碳碳双键,故C错误;
D.苯环上酚羟基邻位氢原子能和溴发生取代反应,碳碳双键和溴发生加成反应,苯环和碳碳双键能和氢气在一定条件下发生加成反应,所以1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别是3mol、4mol,故D正确;
故选BD.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酚、烯烃性质,注意判断原子共面个数的方法,易错选项是C.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
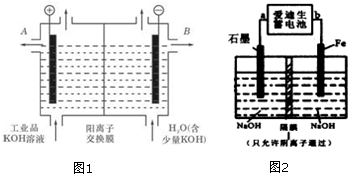
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | Cl2有漂白性 | Cl2能使品红溶液褪色 |
| C | 浓硫酸有脱水性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
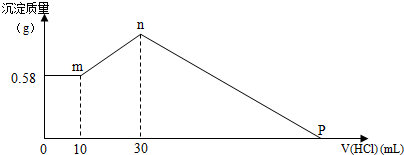
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
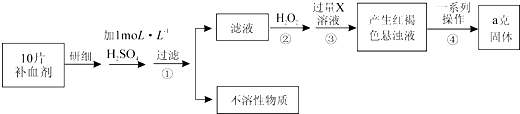
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.05mol/L | B. | 0.1mol/L | C. | 0.2mol/L | D. | 0.3mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②③ | C. | ①⑤ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
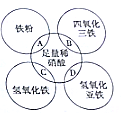 已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )
已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )| A. | Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | Fe(OH)3+3H+═Fe3++3H2O | |
| D. | 3Fe(OH)2+10H++NO3-═3Fe3++NO↑+8H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com