
| A. | 人类目前所直接利用的能源大部分是由化学反应产生的 | |
| B. | 煤,石油,天然气是当今世界最重要的三种化石燃料 | |
| C. | 最理想的能源是煤炭 | |
| D. | 人体运动所消耗的能量与化学反应有关 |
分析 化学反应伴随能量变化,化学能可转化为热能,煤,石油,天然气是当今世界最重要的三种化石燃料,燃烧时易导致环境污染,应开发清洁能源,以此解答该题.
解答 解:A.当前能源结构中,燃料的燃烧是主要的能量来源,燃烧反应为放热反应,所以人类目前所直接利用的能量大部分是由化学反应产生的,故A正确;
B.煤、石油、天然气是三大化石燃料,目前为能源的主要组成,故B正确;
C.煤炭燃烧易导致大量污染,不是最理想的能源,故C错误;
D.人体在运动时发生一系列的化学反应,消耗能量,如ATP与ADP的相互转化,所以人体运动所消耗的能量与化学反应有关,故D正确.
故选C.
点评 本题考查化学反应与能量变化,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,注意生活中的能源及与人类活动有关的能量变化题目难度不大.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:解答题
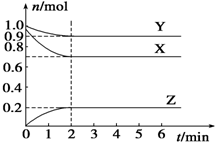 某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 三种酸的酸性为HX<HY<HZ | |
| B. | 物质的量浓度相同的三种盐的水溶液中,NaZ的溶液中,水的电离程度最大 | |
| C. | pH值相同的三种酸的水溶液,恰好中和时所耗NaOH的物质的量为HX<HY<HZ | |
| D. | 物质的量浓度相同的HZ和NaX能发生HZ+NaX=HX+NaZ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | 温度 | 初始pH | 0.1mol/L 草酸溶液/mL | 0.01mol/L KMnO4溶的 体积/mL | 蒸馏水 体积/mL | 待测数据(反应混合液褪色 时间/s) |
| ① | 常温 | 1 | 20 | 50 | 30 | t1 |
| ② | 常温 | 2 | 20 | 50 | 30 | t2 |
| ③ | 常温 | 2 | 40 | a | b | t3 |
| 实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
| 若反应混合液褪色时间小于实验①中的t1,则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com