
| A. | 氮的氧化物可引起光化学烟雾 | |
| B. | 为防止粮食、罐头、水果等食品腐烂,常用氮气做保护气 | |
| C. | SO2可以用作食物和干果的防腐剂 | |
| D. | 铵盐受热易分解,生成氨气和对应的酸 |
分析 A、光化学烟雾的形成与汽车尾气中的氮氧化物有关;
B、作为食品的保鲜措施,需选用性质稳定且成本低的物质,氮气来源广泛且性质稳定;
C、二氧化硫是有毒气体可用于漂白,不能用于食品防腐;
D、铵盐受热易分解,但是不一定得到氨气和对应酸;
解答 解:A、光化学烟雾的形成主要是汽车尾气排放出的氮氧化物发生复杂的变化造成的,故A正确;
B、填充保护气是向其中充入性质稳定,不能与食品发生反应,无毒无味,并且廉价易得的不能供给呼吸的气体,氮气来源广泛且性质稳定常用作保护气,故B正确;
C、二氧化硫是有毒气体可用于漂白,不能用于食品防腐,故C错误;
D、铵盐受热易分解,但是不一定得到氨气和相应的酸,如NH4NO3加热到190℃时分解生成一氧化二氮和水,若加热到300℃左右时分解生成氮气、硝酸和水,故D错误;
故选CD.
点评 本题考查了物质性质的分析应用,主要是物质特征性质的理解应用,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 将铜片置于盐酸中 | B. | 将锌片置于MgCl2溶液中 | ||
| C. | 将铁片置于CuSO4溶液中 | D. | Na2CO3 溶液与CaCl2溶液混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的原子半径比Y的大 | B. | X原子的最外层电子数比Y的大 | ||
| C. | X的原子序数比Y的小 | D. | X元素的最高正价比Y的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽车尾气中发生的催化转化反应:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2 | |
| B. | 工业制氯气:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O | |
| C. | 燃煤时加入石灰石减少SO2排放:2CaCO3+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2 | |
| D. | 用Na2CO3溶液处理水垢中的不溶物CaSO4:CaSO4+CO32-═CaCO3+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂是产生能量最高的营养物质 | |
| B. | 苯能发生氧化反应 | |
| C. | 纤维素可在人体内最终水解成葡萄糖 | |
| D. | 谷氨酸分子中含有2种官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝与氨水反应:Al3++3 OH-═Al(OH)3↓ | |
| B. | 硅酸钠溶液中通入CO2气体:SiO32-+H2O+CO2═H2SiO3↓+CO32- | |
| C. | 饱和NH4Cl溶液中加入NaOH浓溶液:NH4++OH-═NH3↑+H2O | |
| D. | 氯气通入FeCl2溶液中:2Fe2++Cl2═2 Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH | B. | Ba(OH)2 | C. | KSCN | D. | BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
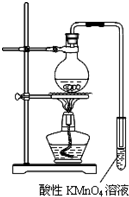 某学习小组探究溴乙烷的消去反应并验证产物.实验原理:CH3CH2Br+NaOH $\stackrel{醇△}{→}$CH2=CH2↑+NaBr+H2O
某学习小组探究溴乙烷的消去反应并验证产物.实验原理:CH3CH2Br+NaOH $\stackrel{醇△}{→}$CH2=CH2↑+NaBr+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若M与W组成原子数为1:1、1:2型离子化合物,则W2G的水溶液含7种粒子 | |
| B. | 若W单质在QM2气体中燃烧生成黑色、白色两种固体,则W的原子序数与族序数之比为5 | |
| C. | 若W与G组成的化合物在水中剧烈反应,产生白色沉淀和气体,M与W组成的化合物易升华 | |
| D. | 若M与W组成的化合物作光导纤维材料,则W单质及其氧化物都抗所有酸溶液的腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com